Болезнь Фабри (БФ) является лизосомной болезнью накопления, приводящей к прогрессирующим нарушениям функционирования нервной системы, почек и сердца. Ферментозаместительная терапия (ФЗТ) способна остановить или замедлить развитие болезни. Поскольку терапия характеризуется сложностью введения препаратов и дороговизной, необходимо определить правильное применение. Наша цель состояла в формулировке согласованных европейских рекомендаций по началу и отмене ФЗТ у пациентов с БФ.
Методы:
Посредством онлайн-опроса (n = 28) и личной встречи (n = 15) было проведено исследование методом Дельфи. На встрече присутствовали представители организации пациентов, выразившие свою точку зрения. Рекомендации были приняты с согласием ≥ 75 % и в отсутствие несогласных.
Результаты:
Было достигнуто соглашение о том, что у мужчин с классическим формой болезни рекомендуется проводить ФЗТ как можно раньше при появлении первых клинических признаков поражения почек, сердца или головного мозга, однако возможность проведения ФЗТ также можно рассматривать в отсутствие клинических признаков или симптомов поражения органов у мужчин в возрасте ≥ 16 лет. У женщин с классической формой БФ и мужчин с неклассической формой БФ лечение следует начинать при появлении ранних клинических признаков поражения почек, сердца или головного мозга. Для женщин с неклассической формой БФ при ранних клинических признаках, предположительно связанных с БФ, можно рассмотреть целесообразность проведения ФЗТ. Было достигнуто соглашение о том, что не следует проводить лечение пациентов с тяжелой почечной недостаточностью (СКФ < 45 мл/мин/1,73 м2), пациентов, проходящих диализ, и пациентов со снижением когнитивных способностей, однако ко всем таким случаям необходимо подходить индивидуально. Отмену ФЗТ можно рассматривать для пациентов с последней стадией БФ или другими смертельными заболеваниями, приводящими к ожидаемой продолжительности жизни < 1 года. У пациентов со снижением когнитивных способностей или отсутствием ответа на лечение в течение 1 года и единственным показанием для ФЗТ в виде нейропатических болей также можно рассмотреть отмену ФЗТ. Также отмену ФЗТ следует рассмотреть у пациентов с терминальной стадией почечной недостаточности без возможности трансплантации почки в сочетании с сердечной недостаточностью поздней стадии (NYHA класс IV). ФЗТ следует отменить у пациентов, не соблюдающих указания или нерегулярно посещающих врача.
Заключение:
Рекомендации можно использовать в качестве критериев начала и отмены ФЗТ, однако конечное решение необходимо принимать в индивидуальном порядке. Для оптимизации данных рекомендаций необходима дальнейшая согласованная работа.
Диагностические критерии и методы лечения часто становятся предметом споров и дискуссий. Это особенно справедливо для редких болезней, включая Болезнь Фабри. Европейская рабочая группа по болезни Фабри (ЕРГБФ) является независимой организацией, состоящей преимущественно из врачей, занимающихся лечением БФ в Европе. В данной статье мы представляем результаты для согласованных рекомендаций по началу и отмене ФЗТ при БФ, полученные врачами ЕРГБФ с учетом комментариев представителей пациентов.
Болезнь Фабри
БФ представляет собой лизосомную болезнь накопления с Х-сцепленным типом наследования, встречающуюся у 1:40000-170000 новорожденных [1-3]. Обычно болезнь проявляется в более позднем возрасте [4]. Болезнь вызывается недостатком лизосомной гидролазы, α- галактозидазы A (AGAL-A), что приводит к накоплению глоботриаозилцерамида (Gb3) [5,6]. К настоящему времени было описано более 600 вариантов гена α-галактозидазы A (GLA), большинство из которых встречаются в пределах отдельных семей [1]. У гемизиготных мужчин болезнь может проявиться в детстве или в раннем подростковом возрасте в форме нейропатических болей, гипо- или ангидроза, диффузной ангиокератомы, воронковидной кератопатии и микроальбуминурии. В более позднем возрасте могут наблюдаться прогрессирующие почечная недостаточность, гипертрофическая кардиомиопатия и нарушения мозгового кровообращения (включая инсульты). Данный фенотип заболевания в настоящее время носит название классической формы БФ. Болезнь также может затрагивать гетерозиготных женщин, однако в таких случаях фенотип более разнообразный, и степень выраженности слабее. Как у мужчин, так и у женщин снижается продолжительность жизни, однако у мужчин это явление выражено сильнее [7,8].
Возраст проявления и прогрессирования болезни значительно варьирует как в пределах одной семьи, так и при сравнении разных семей [9]. В последние пять лет было показано, что у некоторых мужчин с доказанной вызывающей болезнь мутацией гена GLA и сниженной активностью AGAL-A не проявляются все признаки и симптомы классической формы БФ [1]. Данный фенотип называют неклассической формой БФ. У пациентов с неклассической БФ может проявляться один неспецифический симптом, например, хроническая почечная недостаточность или гипертрофия левого желудочка (ГЛЖ). Такие пациенты и женщины с БФ вносят значительный вклад в фенотипическую гетерогенность БФ. С другой стороны, неправильная постановка диагноза болезни Фабри пациентам с аллелью неопределенной значимости (АНЗ) создает дополнительные сложности [4] (см. также таблицу 1) и может привести к началу ферментозаместительной терапии в случаях, когда к этому нет показаний.
Для лечения БФ была разработана ФЗТ агалсидазой альфа или агалсидазой бета. В 2001 году Европейское агентство по лекарственным средствам разрешило использование обеих агалсидаз «в исключительных случаях», то есть соискатель не был способен предоставить исчерпывающих данных об эффективности и безопасности лекарства, поскольку БФ является очень редким заболеванием. Доза агалсидазы альфа составляет 0,2 мг/кг (компания Shire, Лексингтон, Массачусетс, США), доза агалсидазы бета составляет 0,3 – 1,0 мг/кг (компания Genzyme, входящая в Sanofi, Кембридж, Массачусетс, США). В настоящее время ни в одном прямом сравнительном исследовании двух ферментов не было показано превосходства или не меньшей эффективности одного из них [10,11]. В общем случае ФЗТ способна привести к уменьшению сердечной массы [12-15] и снижению накопления Gb3 в почках [16-18], однако влияние на нарушения нервной системы и функцию почек менее очевидно [15,19-22]. Помимо этого, воздействие лечения на пациентов с неклассической формой БФ обычно не исследуется отдельно, и результаты для таких пациентов могут усложнить трактовку исходов лечения. Последние исследования фокусировались на специфических признаках, например, фиброзе сердца или тяжелой почечной недостаточности, способных снизить эффективность ФЗТ, поскольку наличие таких признаков указывает на необратимое повреждение органов [17,19,23]. На основе полученных данных часто рекомендуется раннее начало терапии. Однако термин «раннее начало терапии» до сих пор не был определен. Помимо этого, стоит вопрос, существует ли польза от лечения у пациентов в последней стадии болезни и пациентов, страдающих другими смертельными заболеваниями. Существует несколько местных и национальных руководств и протоколов, содержащих критерии начала и, в редких случаях, отмены ФЗТ, но международный консенсус до сих пор достигнут не был.
Пациенты:
Людей с мутацией гена GLA без проявления характерных фенотипических или биохимических признаков БФ часто сложно диагностировать. Для целей данной консенсусной процедуры обсуждались только пациенты с достоверным диагнозом БФ. Критерии диагностики были рассмотрены в отдельном исследовании, см. таблицу 1 [24].
Таблица 1 Диагностические критерии для достоверной диагностики БФ (взято из Smid и др. с разрешения авторов [24])
 *Определения:
*Определения:
Нейропатическая боль при болезни Фабри удовлетворяет «характерным клиническим критериям», если нейропатическая боль наблюдается в руках и/или стопах, начинается в возрасте до 18 лет и усиливается при жаре, лихорадке. Количественное сенсорное тестирование (КСТ) показывает пониженный порог регистрации холода и повышенную плотность внутриэпидермальных нервных волокон. Другие причины нейропатических болей отсутствуют.
Ангиокератома удовлетворяет «характерным клиническим критериям», если она проявляется скоплениям в характерных областях: на нижней части туловища, губах и вокруг пупка. Другие причины ангиокератомы отсутствуют.
Воронковидная кератопатия удовлетворяет «характерным клиническим критериям», если наблюдаются воронковидные отложения в роговице глаза. Другие причины кератопатии отсутствуют (пациент не принимает препараты, способные вызвать кератопатию, например, Амиодарон, Хлорохин).
**Алгоритмы для отдельных органов см. в Смид и др. [24] и Ван дер Толь и др. [41]. Мутация GLA = мутация гена α-галактозидазы A; AGAL-A = лизосомная гидролаза α-галактозидаза A; БФ = болезнь Фабри; Gb3 = глоботриаозилцерамид; ГЛЖ = гипертрофия левого желудочка; АНЗ = аллель неопределенной значимости.
Процедура разработки согласованного заключения.
Для участия в процедуре разработки согласованного решения были приглашены врачи и исследователи, участвующие в повседневном уходе за пациентами с БФ (n = 41). Их попросили прислать местные или национальные документы, содержащие информацию об используемых в их стране критериях начала и отмены терапии. Экспертов (n = 28) попросили в письменной форме раскрыть любые конфликты интересов (см. конфликты интересов). Для разработки группового соглашения о начале и отмене ФЗТ при БФ использовался модифицированный метод Дельфи. На первом этапе командой исследователей (МБ, КХо) был составлен справочный документ, содержащий информацию о национальных и местных протоколах лечения, обзор критериев включения и исключения испытуемых рандомизированных клинических испытаний и выдержку исследований, затрагивающих проблему ограниченной эффективности ФЗТ у пациентов с нарушениями почек и сердца, потенциально влияющими на исход ФЗТ (результаты литературного обзора представлены в дополнительном документе 1). Также в документ были включены исследования влияния ФЗТ на головной мозг (ТИА/инсульты, поражение белого вещества) [12,19-23] и боли [25,26], исследования эффективности ФЗТ у детей [27-32] и два исследования эффективности антител [33,34]. Затем для обсуждения критериев начала и отмены ФЗТ командой исследователей был составлен онлайн-опросник. Участников экспертной группы попросили оценить критерии по 5-балльной шкале Лайкерта (1 = полностью не согласен, 2 = не согласен, 3 = затрудняюсь ответить, 4 = согласен, 5 = полностью согласен) и добавить свои комментарии и предложения. После проведения опроса была организована личная встреча с представлением и обсуждением анонимных результатов (абсолютных значений и комментариев). Для участия в обсуждении были приглашены представители пациентов из Международной сети болезни Фабри (МСБФ) и Группы поддержки и информирования по болезни Фабри из Нидерландов (ГПИБФН). После обсуждения содержание рекомендаций было соответствующим образом изменено, и участники экспертной группы вновь голосовали по 5-балльной шкале Лайкерта. Конечные рекомендации были составлены после рассылки черного манускрипта участникам экспертной группы и учета из замечаний, присланных по электронной почте.
Статистические аспекты
Критерий включался в рекомендации по лечению, только если наблюдалось согласие 75 % и отсутствовало несогласие (т.е. > 75 % участников экспертной группы проголосовали 1 или 2, и никто не проголосовал 4 или 5, и наоборот).
Результаты
Экспертная группа по разработке согласованного заключения
Был составлен список врачей и исследователей, участвующих в повседневном уходе за пациентами с БФ. Данный список состоял из 41 эксперта, высказавшего интерес во вступлении в ЕРГБФ или известного вкладом в обсуждаемую область. Двадцать восемь экспертов (68 %) заполнили онлайн-опросник и 15 (37 %) участвовали в личной встрече. Четыре представителя пациентов из МСБФ и ГПИБФН (КЛ, ЛБ, АСв, ЭМ) приняли участие во встрече и обсуждениях. Все эксперты и представители пациентов высказали свое мнение о черновом манускрипте, который затем был исправлен в соответствии с полученными замечаниями. В конце концов, все эксперты согласились с результатами, представленными в данном отчете.
Классы рекомендаций
В ходе личной встречи было принято решение классифицировать силу рекомендаций по шкале, описанной в таблице 2 [35]. Рекомендации были изменены в соответствии с этой шкалой. Необходимо отметить, что классификация основывалась, преимущественно, на клиническом опыте, неэкспериментальных исследованиях и ограниченном числе рандомизированных направленных исследований, в которых в основном использовались суррогатные точки клинической эффективности.
Общее заключение
Онлайн-опросник состоял из 57 утверждений. В ходе личной встречи были обсуждены и изменены 34 (60 %) из 57 утверждений, и одно утверждение было добавлено. В результате было получено 58 утверждений, из которых 35 (60 %) были обсуждены в ходе встречи. Сначала утверждение формулировалось как рекомендация класса I (т.е. «рекомендуется лечение ФЗТ» или «рекомендуется отмена лечения ФЗТ»). Если при обсуждении утверждения не было достигнуто соглашение, класс рекомендации снижался (классы IIA и IIB). Если соглашение не было достигнуто даже при формулировке утверждения в качестве рекомендации класса IIB (т.е. «следует рассмотреть начало лечения ФЗТ» или «следует рассмотреть отмену лечения ФЗТ»), делался вывод, что для данного утверждения соглашения достигнуть невозможно. Соглашение было достигнуто для 30 (86 %) из 35 утверждений (см. дополнительный файл 2: таблица S1 и дополнительный файл 3: таблица S2). Шесть (10 %) из остальных 23 утверждений были опущены, поскольку экспертная группа решила, что они не относятся к рассматриваемой проблеме, и 17 (29 %) были рассмотрены в контексте других утверждений или не обсуждались в ходе личной встречи в связи с ограничениями по времени.
Единые критерии начала ФЗТ
Экспертная группа пришла к заключению, что необходимо различать мужчин и женщин, страдающих БФ, и классическую и неклассическую формы БФ. Разделение женщин на пациентов с классической и неклассической формами БФ основывается на наличии или отсутствии диффузной ангиокератомы, воронковидной кератопатии или очень высокого уровня (лизо)Gb3. Для мужчин с классической формой БФ экспертная группа заключила, что проведение ФЗТ можно рассматривать для пациентов старше 16 лет, даже в отсутствие симптомов или клинических признаков поражения органов (рекомендация класса IIB). Диагноз классической БФ у таких пациентов основывается на наличии мутации GLA, отсутствии или очень низкой остаточной активности фермента и наличии одного или нескольких следующих признаков: ангиокератома, воронковидная кератопатия или очень высокий уровень (лизо)Gb3. Лечение мужчин и женщин с классической формой БФ и мужчин с неклассической формой БФ необходимо начинать при первых признаках поражения органов (почек, сердца и/или ЦНС), соответствующих течению БФ и необъяснимых другими патологиями (рекомендация класса I). Можно рассмотреть лечение женщин с неклассической формой БФ и ранними клиническими признаками, указывающими на БФ (рекомендация класса IIB). Критерии начала лечения по отдельным органам описаны в таблице 3.
Утверждение о наличии гиперфильтрации (СКФ > 130 мл/мин/1,73 м2 с корректировкой по возрасту (> 40 лет: –1 мл/мин/1,73 м2/год [36])) как причины начала ФЗТ было опущено, поскольку клиническая значимость данного показателя неоднозначна. Участники экспертной группы пришли к заключению, что не следует отменять лечение пациентов с тяжелой почечной недостаточностью (СКФ < 45 мл/мин/1,73 м2 с корректировкой по возрасту (> 40 лет: –1 мл/мин/1,73 м2/год)). Аналогично, было решено, что не следует отменять лечение пациентов на диализе, даже если они не подходят для трансплантации почки, и пациентов со снижением когнитивных способностей любой этиологии. Начало и продолжение лечения ФЗТ у таких пациентов должно рассматриваться в индивидуальном порядке. Было отмечено, что лечение требует информированного согласия, предпочтительно со стороны пациента (рекомендация класса I).
Единые критерии отмены или отказа в начале ФЗТ
Критерии отмены или отказа в начале ФЗТ приведены в таблице 4. Данные критерии действуют для мужчин и женщин с классической и неклассической формами болезни, за исключением критерия «отсутствие ответа в случае единственного показания нейропатической боли для проведения ФЗТ», который применим ко всем, кроме мужчин с классической формой ФЗТ. Данное исключение основывается на том, что у мужчин с классической БФ и нейропатической болью повышен риск быстрого развития клинических признаков поражения органов.
Таблица 2 Классы рекомендаций
 Таблица 3 Единые критерии начала ФЗТ
Таблица 3 Единые критерии начала ФЗТ
*соответствует БФ и не объясняется другими патологиями; †согласно международным руководствам для заболеваний почек, критерии KDIGO; #в мл/мин/1,73 м2 с корректировкой по возрасте (> 40 лет: –1 мл/мин/1,73 м2/год); $синусовая брадикардия, МА, нарушения реполяризации; ФЗТ = ферментозаместительная терапия; СКФ = скорость клубочковой фильтрации; МТС = максимальная толщина стенки; ЦНС = центральная нервная система; ПБВ = поражение белого вещества; ТИА = транзиторная ишемическая атака; ЖКТ = желудочно-кишечный тракт.
 Таблица 4 Единые критерии отмены или отказа в начале ФЗТ
Таблица 4 Единые критерии отмены или отказа в начале ФЗТ
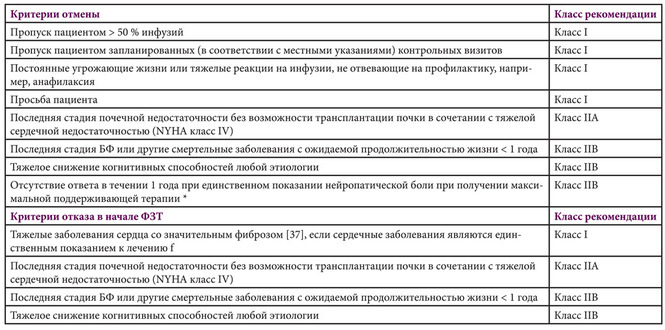
Лечение ФЗТ не рекомендуется в случае только сердечных показаний (т.е. другие признаки или симптомы, для которых может быть рекомендовано лечение, отсутствуют) у пациентов с БФ и тяжелыми заболеваниями сердца со значительным фиброзом [37], соответствующим БФ и не объяснимым другими патологиями.
Утверждения, по которым не было достигнуто соглашения
В дополнительном документе 4: таблица S3 перечислены утверждения, по которым не было достигнуто соглашения. Участники экспертной группы подробно обсудили время начала ФЗТ у молодых мужчин с классической формой БФ без проявления симптомов и клинических признаков поражения органов. Все участники обсуждения согласились, что лечение не следует начинать у пациентов в возрасте 0-5 лет, и можно рассмотреть начало лечения у пациентов старше 16 лет. Однако некоторые участники выступили за начало лечения в возрасте 6-10 лет (33 %) или 11-15 лет (47 %).
Соглашение не было достигнуто в вопросе рекомендации ФЗТ для пациентов с БФ и ранними признаками заболеваний сердца (неуточненных), однако экспертная группа согласилась с более точной формулировкой нарушений сердца как критерия начала ФЗТ (см. таблицу 3). Также обсуждалось, может ли показанное при биопсии почки накопление подоцитов, являющееся единственным признаком поражения органа, быть достаточной причиной начала ФЗТ. Две трети экспертной группы не согласились с данным критерием, одна треть не выразила точного мнения.
Было обсуждено утверждение о том, что ФЗТ не рекомендуется при показании поражения почек у мужчин с классической формой БФ и почечной недостаточностью (СКФ < 45 мл/мин/1,73 м2 с корректировкой по возрасту (> 40 лет: –1 мл/мин/1,73 м2/год)). Сорок процентов согласились с данным утверждением, 20 % не согласились. Остальные 40 % не высказали однозначного мнения. Большинство участников экспертной группы (87 %) согласились, что лечение ФЗТ можно рассмотреть у пациентов с тяжелой почечной недостаточностью (СКФ < 45 мл/мин/1,73 м2 с корректировкой по возрасту (> 40 лет: –1 мл/мин/1,73 м2/год)). Однако 1 участник экспертной группы считал, что у таких пациентов функция почек будет ухудшаться вне зависимости от лечения, и соглашение достигнуто не было.
Вопросы, поднятые представителями пациентов
Представители пациентов выразили озабоченность в связи с утверждением об отмене лечения ФЗТ у пациентов с БФ и повторными инсультами. Представители пациентов указали на то, что в такой ситуации может сохраняться высокое качество жизни, и пациенты могут получить пользу от лечения. Было решено исключить данное утверждение. Сходные рассуждения применимы к пациентам со снижением когнитивных способностей. После обсуждения было решено, что лечение нельзя не предоставлять пациентам со снижением когнитивных способностей любой этиологии (включая повторные инсульты), однако был сделан акцент на необходимости получения согласия на лечение, предпочтительно от пациента (рекомендация класса I). Помимо этого, было решено, что у пациентов с сильным снижением когнитивных способностей можно рассмотреть отмену лечения (рекомендация класса IIB), однако было отмечено, что отмена ФЗТ в данном случае должна рассматриваться в индивидуальном порядке.
Было достигнуто согласие в вопросе о том, что ФЗТ следует отменять у пациентов, не соблюдающих режим лечения (пропустивших > 50 % инфузий) или пропускающих плановые визиты к врачу (рекомендации класса I).
Обсуждение
Существует несколько местных и национальных протоколов, содержащих различные наборы критериев начала и/или отмены ФЗТ при БФ. Расхождения между протоколами объясняются, в основном, ограниченным объемом данных о лечении. Используя модифицированный метод Дельфи, экспертная группа, состоящая из европейских экспертов по БФ, рассмотрела рекомендации начала и отмены ФЗТ на основе действующих стандартов доказательной науки и практики. В рассмотрение были включены предложения организации пациентов, страдающих БФ.
Следует отметить, что наши рекомендации применимы только к пациентам с достоверным диагнозом БФ в соответствии с определениями, приведенным в таблице 1. Необходимо избегать ФЗТ у пациентов без БФ [4]. Наш метод привел к разделению мужчин и женщин, страдающих БФ, и классической и неклассической форм БФ. В общем случае, рекомендуется начинать ФЗТ при первых признаках поражения почек, сердца или головного мозга, соответствующих диагнозу БФ. У мужчин с классической формой БФ начало ФЗТ можно рассмотреть в отсутствие клинических признаков или симптомов. При этом рекомендации начала ФЗТ у женщин с неклассической формой БФ и ранними клиническими признаками болезни менее строгие. Наши рекомендации о начале ФЗТ при первых клинических признаках БФ основываются на исследованиях, демонстрирующих, что характерные свойства прогрессирующего заболевания, например, фиброз сердца или тяжелые нарушения функции почек, могут снизить эффективность ФЗТ. Наличие таких нарушений может указывать на необратимое повреждение органов [17,19,23]. На основе известных данных рекомендуется раннее начало терапии. Однако в ходе обсуждения оказалось, что участники экспертной группы по-разному понимают «ранее начало». Некоторые участники считали, что лечение мужчин с классической формой болезни следует начинать в возрасте 6-10 лет. По их мнению, с метаболической точки зрения лечение необходимо начинать как можно раньше. Однако другие эксперты считали, что следует дождаться проявления признаков или симптомов поражения органов, поскольку данные о пользе начала ФЗТ в бессимптомном состоянии отсутствуют. Более того, педиатры заключили, что раннее начало ФЗТ у бессимптомных детей в контексте очень медленно прогрессирующей болезни может помешать нормальному детству. В конце концов, экспертная группа пришла к заключению, что при отсутствии признаков и симптомов начало ФЗТ можно рассмотреть (рекомендация класса IIB) у мужчин с классической формой БФ старше 16 лет. Однако необходимо отметить, что у большинства мужчин с классической формой болезни признаки и симптомы проявляются до 16 лет. Единые рекомендации по началу лечения мальчиков младше 16 лет с классической формой болезни без признаков и симптомов могут быть обновлены, если появятся данные, поддерживающие ранее начало ФЗТ у детей (www.clinicaltrials.gov, номер клинического исследования: NCT00701415).
В ходе обсуждения было отмечено, что признаки поражения органов являются показанием к началу ФЗТ только, если поражение органов соответствует картине БФ. Таким образом, для всех пациентов для идентификации вызванного БФ поражения органов и других причин нарушения функций почек, сердца и головного мозга, необходимо проводить подробный медицинский осмотр и биохимические анализы. Это означает, что в некоторых случаях требуется биопсия органов. Например, если единственным признаком поражения органов является гипертрофия левого желудочка, необходимо рассмотреть возможность проведения эндомиокардиальной биопсии, особенно, если у пациента наблюдаются сопутствующие факторы риска сердечно-сосудистых заболеваний. Электронно-микроскопическое исследование биопсии позволяет определить причину поражения органа. Однако, если наблюдается характерное для БФ накопление, то гипертрофия по крайней мере частично вызвана БФ, и рекомендуется начать ФЗТ.
Наши рекомендации основываются на предположении, что пациенты получают оптимальную поддерживающую терапию. В соответствии с указаниями по лечению хронических заболеваний почек (KDIGO) [38] и сердечно-сосудистых заболеваний (ESC) [39] при начале ФЗТ необходимо начать или продолжить терапию ингибиторами ангиотензинпревращающего фермента (ACE) или блокаторами рецептора ангиотензина II (ARB). Согласно указаниям AHA/ASA по предупреждению повторных инсультов [40], если пациент перенес инсульт или транзиторную ишемическую атаку, необходимо начать антитромбоцитарную терапию и прием статинов. Если пациент страдает от нейропатических болей, могут понадобиться обезболивающие препараты.
Данные рекомендации основаны на экспертных мнениях и знаниях, полученных в неэкспериментальных исследованиях, поскольку данных уровня А (т.е. данных рандомизированных направленных исследований) в настоящее время очень мало. Для определения эффективности ФЗТ у пациентов с разными степенями поражения почек, сердца и головного мозга требуются дальнейшие исследования. Например, участники экспертной группы не пришли к соглашению о пороговом значении СКФ, ниже которого почечная недостаточность может считаться необратимой. Некоторые эксперты считали, что ФЗТ не рекомендуется при СКФ ниже 45 мл/мин/1,73 м2 с корректировкой по возрасту (> 40 лет: –1 мл/мин/1,73 м2/год), когда как другие утверждали, что при СКФ ниже 45 мл/мин/ 1,73 м2 возможно значительное улучшение. На данный момент нет исследований, однозначно разрешающих эту дилемму. Помимо этого, стандартные процедуры контрольных осмотров различаются в разных центрах. Например, для диагностирования фиброза сердца использовались определенные аппараты для измерения сердечного магнитного резонанса [37]. Необходимо исследовать вопрос о том, можно ли экстраполировать результаты из одного центра на другие.
Заключение
Наши рекомендации необходимо интерпретировать в контексте ограниченного объема знаний, то есть в случае публикации результатов клинических исследований их необходимо пересмотреть. Более того, рекомендации не дают простых однозначных правил. Их необходимо рассматривать в качестве общих принципов начала или отмены ФЗТ у пациентов с БФ, и конечное решение должно приниматься с учетом характеристик БФ, сопутствующих заболеваний и личных предпочтений. ЕРГБФ собирается регулярно обновлять рекомендации и служить независимым источником помощи врачам, заботящимся о пациентах с БФ.
Дополнительные документы
Дополнительный документ 1: Результаты обзора литературы для встречи Европейской рабочей группы по болезни Фабри (ЕРГБФ), посвященной составлению единых рекомендаций по началу и отмене ферментозаместительной терапии (агалсидаза альфа и агалсидаза бета) у пациентов с болезнью Фабри.
Дополнительный документ 2: Таблица S1. Утверждения о начале ФЗТ, по которым было достигнуто согласие.
Дополнительный документ 3: Таблица S2. Утверждения об отмене или отказе в начале ФЗТ, по которым было достигнуто согласие.
Дополнительный документ 4: Таблица S3. Утверждения, по которым не было достигнуто согласие.
Сокращения
БФ: болезнь Фабри; мутация GLA: мутация гена α-галактозидазы A; AGAL-A: лизосомная гидролаза α-галактозидаза A; Gb3: глоботриаозилцерамид; АНЗ: аллель неопределенной значимости; ФЗТ: ферментозаместительная терапия; ЕРГБФ: Европейская рабочая группа по болезни Фабри; МСБФ: Международная сеть болезни Фабри; ГПИБФН: Группа поддержки и информирования по болезни Фабри из Нидерландов; СКФ: скорость клубочковой фильтрации; ГЛЖ: гипертрофия левого желудочка; МТС: максимальная толщина стенки; NYHA: Нью-Йоркская кардиологическая ассоциация; ЦНС: центральная нервная система; ПБВ: поражение белого вещества; ТИА: транзиторная ишемическая атака; ЖКТ: желудочно-кишечный тракт; ACE: ангиотензинпревращающий фермент; ARB: блокатор рецептора ангиотензина II.
Конфликты интересов
- МБ, ГЛ и КХо получали средства для проведения исследований, образовательные гранты, командировочные, гонорары за консультации и публичные выступления от компаний Genzyme, Shire HGT, Amicus, Protalix и Actelion. Все гонорары были переданы в фонды Gaucher Stichting и AMC Medical Research для финансирования исследований.
- ФБ получил исследовательский грант от компании Shire HGT.
- ФЦ получал гонорары за лекции и исследовательские гранты от компании Genzyme.
- ПД получал средства для проведения исследований, командировочные и гонорары за публичные выступления от компаний Genzyme и Shire.
- УФР получала гонорары за лекции и участие в экспертных советах от компаний Genzyme, Shire HGT и Amicus.
- ТГ и ДЖ получали исследовательские гранты и командировочные от компаний Genzyme и Shire HGT.
- ДХ получала гранты на оплату командировок и исследований и гонорары за лекции и участие в экспертных советах от компаний Genzyme, Shire HGT, Amicus и Protalix.
- ИК получал командировочные от компаний Genzyme и Shire HGT.
- АМ получал исследовательские гранты от компаний Genzyme, Shire HGT, Amicus и Protalix, и гонорары от компаний Genzyme и Shire HGT.
- ХО получал командировочные от компаний Genzyme, Shire HGT и Amicus и гонорары за публичные выступления и средства для проведения исследований от компании Genzyme.
- РП получала гонорары от компаний Genzyme и Shire HGT.
- УР получала гонорары за консультации от компаний Shire HGT и Raptor Pharmaceuticals и командировочные и гонорары за публичные выступления от компаний Shire HGT и Biomarin.
- АСе получал исследовательские гранты от компаний Shire и Genzyme.
- КС получила неограниченный образовательный грант и гонорары за публичные выступления от компании Genzyme, и гонорары от компаний Pfizer, Baxter и CSL Behring.
- ГСП получал гонорары за публичные выступления, командировочные и исследовательские гранты от компаний Genzyme и Shire и гонорары от компании Amicus.
- ЭС и КТ получали гонорары за публичные выступления от компаний Genzyme и Shire HGT.
- БВ получал командировочные и гонорары за публичные выступления от компаний Genzyme и Shire HGT и гонорары за участие в экспертных советах от компании Genzyme.
- ФАВ получал командировочные, гонорары за публичные выступления и исследовательские гранты от компаний Genzyme и Shire HGT и гонорары за участие в экспертных советах от компании Genzyme.
- ФВ получал исследовательские гранты, командировочные, гонорары за консультации и публичные выступления от компаний Genzyme, Shire HGT, Biomarin и Actelion.
- ПВ получал гонорары за лекции и участие в экспертных советах от компании Genzyme.
- Организация МСБФ получала неограниченные образовательные гранты и средства на командировки от компаний Genzyme, Shire HGT, Amicus, Synageva, Biomarin и Patbio для обеспечения деятельности по защите прав больных.
- Организация ГПИБФН получала неограниченные образовательные гранты от компаний Genzyme, Shire HGT, Amicus и GSK для обеспечения деятельности по защите прав больных.
- У РА, КХе, НК, МР, ВТ и АТЖ конфликты интересов отсутствуют.
Вклад авторов
МБ и КХо участвовали в разработке и организации исследования и составили черновой манускрипт. КХо и ГЛ составили опросник. РА, ФБ, ЛБ, ТГ, ДЖ, ДХ, ИК, КЛ, АМ, ЭМ, УР, МР, ЭС, АСв, ВТ, КТ, АТЖ и БВ заполнили онлайн-опросник и приняли участие в личной встрече. ПД, УФР, КХе, НК, ХО, РП, Асе, КС, ГСП, ФАВ, ФВ и ПВ заполнили онлайн-опросник. Все авторы прочитали и одобрили конечный манускрипт.
Благодарности
Мы хотим поблагодарить Бовиен Смид, Линду ван дер Толь и Маартена Арендса за поддержку в ходе личной встречи и Аннелис Керс за работу над справочным документом. Мы также благодарим проф. др. К. Уэннера за участие в онлайн-опросе.
Данное исследование проводилось на средства гранта Министерства здравоохранения (ZonMw). Исследователи работали независимо от финансирующей стороны. Источник финансирования не участвовал в разработке исследования, сборе, анализе и интерпретации данных, написании отчета и принятии решения о публикации статьи.
Информация об авторах
1Кафедра болезней внутренних органов, отделение эндокринологии и метаболизма, Академический медицинский центр, а/я 22660, Амстердам 1100 DD, Нидерланды. 2Биомедицинский центр, Исландский университет и Национальная университетская больница, Рейкьявик, Исландия. 3Центр молекулярных заболеваний, Госпитальный университетский центр кантона Во, Лозанна, Швейцария. 4Международная сеть болезни Фабри (МСБФ), Амершем, Великобритания. 5Кафедра клинической и экспериментальной медицины, Флорентийский университет, Флоренция, Италия. 6Кафедра медицины, больница Адденбрука и Кембриджский университет, Кембридж, Великобритания. 7Кафедра медицинской эндокринологии, больница Копенгагенского университета, Копенгаген, Дания. 8Кафедра эндокринологии, университетские больницы фонда Национальной системы здравоохранения в Бирмингеме, Бирмингем, Великобритания. 9Кафедра медицинской генетики, Версальский университет, Монтиньи, Франция. 10Кафедра наследственных метаболических заболеваний взрослых, Академический центр наук о здоровье Манчестера, Манчестер, Великобритания. 11Кафедра гематологии, группа болезней лизосомного накопления, Королевская бесплатная больница, Лондон, Великобритания. 12Отделение медицины, больница университета Турку, Турку, Финляндия. 13Вилла метаболика, Центр педиатрической и подростковой медицины, Майнц, Германия. 14Группа поддержки и информирования по болезни Фабри из Нидерландов (ГПИБФН), Остерволде, Нидерланды. 15Кафедра генетики, Университет Порто и Госпитальный центр Сао-Хоао, Порто, Португалия. 16Группа редких метаболических заболеваний, Университетская больница Сан Жерардо, Монца, Италия. 17Группа лизосомных нарушений, Институт иммунитета и трансплантации, Королевская бесплатная больница, Лондон, Великобритания. 18Кафедра болезней внутренних органов IV, отделение нефрологии и гипертензии, Инсбрукский медицинский университет, Инсбрук, Австрия. 19Институт эпидемиологии, биостатистики и предупреждения, Университет Цюриха, Цюрих, Швейцария. 20Кафедра неврологии, Университет Вюрцбурга, Вюрцбург, Германия. 21Кафедра медицины III, отделение нефрологии и диализа, Венский медицинский университет, Вена, Австрия. 22Кафедра медицины, Университетская больница Хеукелана и кафедра клинической медицины, Университет Бергена, Берген, Норвегия. 23Кафедра болезней внутренних органов, отделение нефрологии, Университетская больница Гента, Гент, Бельгия. 24Кафедра педиатрии, питания и метаболических болезней, Мемориальный институт детского здоровья, Варшава, Польша. 25Группа клинических исследований/кафедра педиатрии, Университетская больница Хеукелана, Берген, Норвегия. 26Больница Словень Градеца, Словень Градец, Словения. 27Клиника внутренних заболеваний II, больница Катаринен в Унне, Унна, Германия. 28Кафедра педиатрии, Академический медицинский центр, Амстердам, Нидерланды. 29Кафедра кардиологии, Королевская больница Салфорда фонда Национальной системы здравоохранения, Манчестер, Великобритания.
Статья получена: 15 января 2015 г.
Статья принята: 15 марта 2015 г.
Статья опубликована онлайн: 27 марта 2015 г.
Список литературы
1. Десник Р.Дж. (Desnick RJ), Ианноу Й.А. (Ioannou YA), Энг М.Э. (Eng ME). Недостаточность α-галактозидазы A: болезнь Фабри, Молекулярные и метаболические основы наследственных заболеваний онлайн. 2007. Стр. 3733-74.
2. Мейкл П.ДЖ. (Meikle PJ), Хопвуд Дж.Дж. (Hopwood JJ), Клаг А.Э. (Clague AE), Кэри У.Ф. (Carey WF) и др. Распространенность болезней лизосомного накопления. JAMA. 1999; 281(3):249-54.
3. Пуртуис Б.Дж. (Poorthuis BJ), Веверс Р.Э. (Wevers RA), Кляйер В.Й. (Kleijer WJ), Гронер Дж.Э. (Groener JE), де Йонг Й.Г. (de Jong JG), ван Уили С. (van Weely S) и др. Частота встречаемости болезней лизосомного накопления в Нидерландах. Hum Genet. 1999; 105(1-2):151-6.
4. Ван дер Толь Л. (Van der Tol L), Смид Б.Э. (Smid BE), Пуртуис Б.Дж.Х.М. (Poorthuis BJHM), Биегштраатен М. (Biegstraaten M), Леканне Депрез Р.Х. (Lekanne Deprez RH), Линтхерст Г.Э. (Linthorst GE) и др. Систематический обзор скрининга болезни Фабри: распространенность людей с аллелями неопределенной значимости. J Med Genet. 2014; 51(1):1-9.
5. Брейди Р.О. (Brady RO), Гэл А.Э. (Gal AE), Бредли Р.М. (Bradley RM), Мартенссон Э. (Martensson E), Варшоу Э.Л. (Warshaw AL), Лэстер Л. (Laster L) и др. Ферментативный дефект при болезни Фабри. Недостаточность церамидтригексозидазы. N Engl J Med. 1967; 276(21):1163-7.
6. Кинт Дж.Э. (Kint JA). Болезнь Фабри: недостаточность альфа-галактозидазы. Science. 1970; 167 (3922):1268-9.
7. МакДермот К.Д. (MacDermot KD), Холмс Э. (Holmes A), Майнерс Э.Х. (Miners AH). Болезнь Андерсона-Фабри: клинические проявления и влияние болезни в когорте 98 гемизиготных мужчин. J Med Genet. 2001; 38(11):750-60.
8. МакДермот К.Д. (MacDermot KD), Холмс Э. (Holmes A), Майнерс Э.Х. (Miners AH). Болезнь Андерсона-Фабри: клинические проявления и влияние болезни в когорте 60 женщин-облигатных носителей. J Med Genet. 2001; 38(11):769-75.
9. Десник Р.Дж. (Desnick RJ), Брейди Р. (Brady R), Берренджер Дж. (Barranger J), Коллинс Э.Дж. (Collins AJ), Гермейн Д.П. (Germain DP), Голдман М. (Goldman M) и др. Болезнь Фабри, недостаточно диагностируемое полиорганное заболевание: экспертные рекомендации для диагностики, ведения и ферментозаместительной терапии. Ann Intern Med. 2003; 138(4):338-46.
10. Веддер А.К. (Vedder AC), Линтхерст Г.Э. (Linthorst GE), Хоудж Г. (Houge G), Гренер Дж.Э. (Groener JE), Ормел Э.Э. (Ormel EE), Бума Б.Дж. (Bouma BJ) и др. Лечение болезни Фабри: результаты сравнительного исследования агалсидазы альфа и агалсидазы бета при дозе 0,2 мг/кг. PLoS One. 2007; 2(7):e598.
11. Сиррс С.М. (Sirrs SM), Бичет Д.Г. (Bichet DG), Кейси Р. (Casey R), Кларк Дж.Т. (Clarke JT), Лемойн К. (Lemoine K), Дусетт С. (Doucette S) и др. Исходы для пациентов, получавших лечение в рамках Канадской инициативы по болезни Фабри. Mol Genet Metab. 2014; 111(4):499-506.
12. Баниказеми М. (Banikazemi M), Балтас Дж. (Bultas J), Вальдек С. (Waldek S), Уилкокс В.Р. (Wilcox WR), Уитли К.Б. (Whitley CB), МакДональд М. (McDonald M) и др. Терапия агалсидазой бета при прогрессирующей болезни Фабри: рандомизированное исследование. Ann Intern Med. 2007; 146(2):77-86.
13. Бирер Г. (Bierer G), Балфе Д. (Balfe D), Уилкокс В.Р. (Wilcox WR), Мозенифар З. (Mosenifar Z) и др. Улучшение результатов кардиопульмональных тестов с физической нагрузкой после ферментозаместительной терапии при болезни Фабри. J Inherit Metab Dis. 2006; 29(4):572-9.
14. Хьюз Д.Э. (Hughes DA), Эллиот П.М. (Elliot PM), Ша Дж. (Shah J), Цукерман Дж. (Zuckerman J), Коглан Г. (Coghlan G), Брукс Дж. (Brookes J) и др. Влияние ферментозаместительной терапии на кардиомиопатию болезни Андерсона-Фабри: рандомизированное двойное слепое плацебо-контролируемое клиническое исследование агалсидазы альфа. Heart. 2008; 94(2):153-8.
15. Ромбах С.М. (Rombach SM), Смид Б.Э. (Smid BE), Линтхерст Г.Э. (Linthorst GE), Дижкграаф М.Г. (Dijkgraaf MG), Холлак К.Э.М. (Hollak CEM) и др. Естественное развитие болезни Фабри и ферментозаместительная терапия: систематический обзор и мета-анализ: эффективность ФЗТ на различных стадиях болезни. J Inherit Metab Dis. 2014; 37(3):341-52.
16. Тарберг Б.Л. (Thurberg BL), Реннке Х. (Rennke H), Колвин Р.Б. (Colvin RB), Дикман С. (Dikman S), Гордон Р.Э. (Gordon RE), Коллинс Э.Б. (Collins AB) и др. Накопление глоботриаозилцерамида удаляется из различных типов клеток почек при болезни Фабри после ферментозаместительной терапии. Kidney Int. 2002; 62(6):1933-46.
17. Гермейн Д.П. (Germain DP), Вальдек С. (Waldek S), Баниказеми М. (Banikazemi M), Бушинский Д.А. (Bushinsky DA), Чарроу Дж. (Charrow J), Десник Р.Дж. (Desnick RJ) и др. Поддерживающаяся, долговременная стабилизация почек после 54 месяцев терапии агалсидазой бета у пациентов с болезнью Фабри. J Am Soc Nephrol. 2007; 18:1547-57.
18. Тондель К. (Tondel C), Боштад Л. (Bostad L), Ларсен К.К. (Larsen KK), Хирт Э. (Hirth A), Виксе Б.Э. (Vikse BE), Хоудж Г. (Houge G) и др. Агалсидаза улучшает гистологию почек у молодых пациентов с болезнью Фабри. J Am Soc Nephrol. 2013; 24(1):137-48.
19. Ромбах С.М. (Rombach SM), Смид Б.Э. (Smid BE), Боувман М.Г. (Bouwman MG), Линтхерст Г.Э. (Linthorst GE), Дижкграаф М.Г. (Dijkgraaf MG), Холлак К.Э. (Hollak CE) и др. Долговременная ферментозаместительная терапия болезни Фабри: эффективность для почек, сердца и головного мозга. Orphanet J Rare Dis. 2013; 8:47.
20. Бухнер С. (Buechner S), Моретти М. (Moretti M), Бурлина А. (Burlina A), Цей Г. (Cei G), Манара Р. (Manara R), Риччи Р. (Ricci R) и др. Поражение центральной нервной системы при болезни Андерсона-Фабри: клиническое и МРТ ретроспективное исследование. J Neurol Neurosurg Psychiatry. 2008; 79(11):1249-54.
21. Жардим Л. (Jardim L), Ведолин Л. (Vedolin L), Шварц И.В. (Schwartz IV), Бурин М.Г. (Burin MG), Цекчи К. (Cecchin C), Калакун Л. (Kalakun L) и др. Поражение ЦНС при болезни Фабри: клинические и визуализационные исследования до и после 12 месяцев ферментозаместительной терапии. J Inherit Metab Dis. 2004; 27(2):229-40.
22. Жардим Л.Б. (Jardim LB), Эссе Ф (Aesse F), Ведолин Л. (Vedolin L), Питта- Пинхейро К. (Pitta-Pinheiro C), Марконато Дж. (Marconato J), Бурин М.Г. (Burin MG) и др. Поражение белого вещества при болезни Фабри до и после ферментозаместительной терапии: контрольное исследование через 2 года. Arq Neuropsiquiatr. 2006; 64(3B):711-7.
23. Видеманн Ф. (Weidemann F), Ниеманн М. (Niemann M), Сторк С. (Stork S), Бреуниг Ф. (Breunig F), Беер М. (Beer M), Соммер К. (Sommer C)и др. Долговременные исходы ферментозаместительной терапии болезни Фабри поздней стадии: данные по прогрессированию заболевания в сторону тяжелых осложнений. J Intern Med. 2013;274(4):331-41.
24. Смид Б.Э. (Smid BE), Ван дер Толь Л. (Van der Tol L), Цекчи Ф. (Cecchi F), Эллиот П.М. (Elliott PM), Хьюз Д.Э. (Hughes DA), Линтхерст Г.Э. (Linthorst GE) и др. Сомнительный диагноз болезни Фабри: единые рекомендации для диагностики взрослых с гипертрофией левого желудочка и аллелью неопределенной значимости. Int J Cardiol. 2014; 177(2):400-8.
25. Шиффман Р. (Schiffmann R), Копп Дж.Б. (Kopp JB), Остин Х.Э.И. (Austin HAI), Сабнис С. (Sabnis S), Мур Д.Ф. (Moore DF), Вибель Т. (Weibel T) и др. Ферментозаместительная терапия при болезни Фабри: рандомизированное направленное исследование. JAMA. 2001; 285:2743-9.
26. Энг К.М. (Eng CM), Гаффон Н. (Guffon N), Уилкокс В.Р. (Wilcox WR), Гремейн Д.П. (Germain DP), Ли П. (Lee P), Вальдек С. (Waldek S) и др. Безопасность и эффективность рекомбинантной человеческой терапии замещения альфа-галактозидазы при болезни Фабри. N Engl J Med. 2001; 345(1):9-16.
27. Рис М. (Ries M), Кларк Дж.Т.Р. (Clarke JTR), Вибра К. (Whybra C), Тиммонс М. (Timmons M), Робинсон К. (Robinson C), Шлаггар Б.Л. (Schlaggar BL) и др. Ферментозаместительная терапия агалсидазой альфа у детей с болезнью Фабри. Pediatrics. 2006; 118:924-32.
28. Рамасвами У. (Ramaswami U), Вендт С. (Wendt S), Пинтос-Морелл Г. (Pintos-Morell G), Парини Р. (Parini R), Вибра К. (Whybra C), Леон Лил Дж.Э. (Leon Leal JA) и др. Ферментозаместительная терапия галсидазой альфа у детей с болезнью Фабри. Acta Paediatr. 2007; 96(1):122-7.
29. Рейф Дж.Э. (Wraith JE), Тилки-Жманьска А. (Tylki-Szymanska A), Гаффон Н. (Guffon N), Льен Й.Х. (Lien YH), Тсимаратос М. (Tsimaratos M), Веллоди Э. (Vellodi A) и др. Безопасность и эффективность ферментозаместительной терапии агалсидазой бета: международное открытое исследование педиатрических пациентов с болезнью Фабри. J Pediatr. 2008; 152(4):563-70.
30. Шифманн Р. (Schiffmann R), Мартин Р.Э. (Martin RA), Раймшизель Т. (Reimschisel T), Джонсон К. (Johnson K), Кастанеда В. (Castaneda V), Льен Й.Х. (Lien YH) и др. Четырехлетнее проспективное исследование терапии агалсидазой альфа детей с болезнью Фабри. J Pediatr. 2010; 156(5):832-7.
31. Рамасвами У. (Ramaswami U), Парини Р. (Parini R) Кампманн К. (Kampmann C), Бек М. (Beck M) и др. Безопасность агалсидазы альфа у пациентов с болезнью Фабри младше 7 лет. Acta Paediatr. 2011; 100(4):605-11.
32. Боргвардт Л. (Borgwardt L), Фельдт-Расмуссен У. (Feldt-Rasmussen U), Расмуссен Э.К. (Rasmussen AK), Баллегаард М. (Ballegaard M), Мельдгаард Лунд Э. (Meldgaard Lund A) и др. Болезнь Фабри у детей: ферментозаместительная терапия агалсидазой бета. Clin Genet. 2013; 83(5):432-8.
33. Ромбах С.М. (Rombach SM), Эртс Дж.М. (Aerts JM), Пуртуис Б.Дж. (Poorthuis BJ), Гренер Дж.Э. (Groener JE), Донкер-Купман В. (Donker-Koopman W), Хендрикс Э. (Hendriks E) и др. Долговременное влияние антител против введенной альфа-галактозидазы A при болезни Фабри на снижение содержания (лизо)Gb3 в плазме и моче и исходы лечения. PLoS One. 2012; 7(10):e47805.
34. Беничу Б. (Benichou B), Гойал С. (Goyal S), Санг К. (Sung C), Норфлит Э.М. (Norfleet AM), О’Брайен Ф. (O’Brien F) и др. Ретроспективный анализ потенциального воздействия антител IgG на эффективность агалсидазы бета при ферментозаместительной терапии. Mol Genet Metab. 2009;96(1):4-12.
35. Монталеско Ж. (Montalescot G), Сечтем У. (Sechtem U), Ахенбах С. (Achenbach S), Андреотти Ф. (Andreotti F), Арден К. (Arden C), Будаж Э. (Budaj A) и др. Указания Европейского общества кардиологов по ведению стабильной ишемической болезни сердца от 2013 года: оперативная группа ведения стабильной ишемической болезни сердца Европейского общества кардиологов. Eur Heart J. 2013; 34(38):2949-3003.
36. Глассок Р.Дж. (Glassock RJ), Уинерлс К. (Winearls C). Старение и скорость клубочковой фильтрации: факты и последствия. Trans Am Clin Climatol Assoc. 2009; 120:419-28.
37. Видеманн Ф. (Weidemann F), Ниманн М. (Niemann M), Брониг Ф. (Breunig F), Херрманн С. (Herrmann S), Беер М. (Beer M), Сторк С. (Stork S) и др. Долговременное влияние ферментозаместительной терапии на кардиомиопатию при болезни Фабри: данные о лучших исходах при раннем начале лечения. Circulation. 2009;119(4):524-9.
38. Руководство по клинической практике KDIGO. http://kdigo.org/home/guidelines/.
39. Руководство по клинической практике ESC. http://www.escardio.org/guidelines.
40. Руководство AHA/ASA. https://www.aan.com/Guidelines/home/GetGuidelineContent/581.
41. Ван дер Толь Л. (Van der Tol L), Сварштад Э. (Svarstad E), Ортиз Э. (Ortiz A), Тондель К. (Tondel C), Оливейра Х.П. (Oliveira JP), Вогт Л. (Vogt L) и др. Хроническая почечная недостаточность и сомнительный диагноз болезни Фабри: подход к правильной диагностике. Mol Genet Metab. 2015; 114(2):242-7.
[/vc_column_text][/vc_column][/vc_row]




