Кистозный фиброз (муковисцидоз) (МВ)
Определение
Муковисцидоз — частое моногенное заболевание, обусловленное мутацией гена трансмембранного регулятора муковисцидоза ( МВТР ), который является каналом для активного перемещения ионов хлора, а также регулятором обратного всасывания ионов натрия и характеризующееся поражением экзокринных желез жизненно важных органов и систем и имеющее обычно тяжелое течение и прогноз.
СКАЧАТЬ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО МУКОВИСЦИДОЗУ
Этиология и патогенез
В результате увеличения обратного всасывания натрия снижается и/или прекращается секреция жидкости, продуцируемый в бронхах секрет теряет жидкую часть и приобретает более густую консистенцию. Дефект секреции хлора влечет за собой повышение вязкости слизи. Степень эластичности слизи и скорость её перемещения зависят от концентрации ионов кальция и магния. При муковисцидозе в патологический процесс в различной степени вовлекается весь организм, но в большей степени страдают органы дыхания, поджелудочная железа, печень, желчевыводящие пути, желудочно — кишечный тракт, потовые железы и половые органы. Больные МВ представляют одну из самых тяжелых категорий пульмонологических пациентов .
 Поражение легких при муковисцидозе, в основе которого лежит хронический инфекционный процесс, по — прежнему остается основной причиной смертности больных. Образующийся вязкий бронхиальный секрет приводит к развитию бронхиальной обструкции, на фоне которой развивается хроническая бронхиальная инфекция.
Поражение легких при муковисцидозе, в основе которого лежит хронический инфекционный процесс, по — прежнему остается основной причиной смертности больных. Образующийся вязкий бронхиальный секрет приводит к развитию бронхиальной обструкции, на фоне которой развивается хроническая бронхиальная инфекция.
Формируется порочный круг: бронхиальная обструкция – инфекция — гиперпродукция слизи — бронхиальная обструкция. Прогноз заболевания определяет интенсивная рациональная антибактериальная терапия, которая направлена на максимально возможное повышение или сохранение легочной функции, минимизацию числа обострений респираторных инфекций, улучшение качества и продолжительности жизни и перспективы для трансплантации легких.
Эпидемиология
Распространенность кистозного фиброза (муковисцидоза) наследуется по аутосомно — рецессивному типу. Муковисцидоз наиболее распространен у лиц европеоидной расы, однако и у них его частота существенно варьируется в различных географических регионах и этнических группах. На современном этапе описано приблизительно 2000 мутаций в гене МВТР, при чем частота и спектр отличается значительными вариациями у различных этнических групп 14 и популяций. Установлено, что каждый 25 — й представитель европеоидной расы является носителем гена муковисцидоза .
 Распространенность муковисцидоза в странах Северной Европы и Северной Америки с оставляет 1 на 2000 — 2500 новорожденных. Так, например, в Ирландии частота муковисцидоза составляет 1: 1800 новорожденных, в Финляндии – 1: 26000. муковисцидоз крайне редок среди коренного населения Азии и Африки (менее 1 на 100 000 ) . По данным эпидемиологических исследований в России частота болезни в различных регионах колеблется от 1:8500 до 1:12900 новорождённых. Если оба родителя гетерозиготные (являются носителями мутировавшего гена), то риск рождения больного муковисцидозом ребёнка составляет 25 %. Носители только одного дефектного гена (аллели) не болеют муковисцидозом. По данным исследований частота гетерозиготного носительства патологического гена равна 2 — 5 %
Распространенность муковисцидоза в странах Северной Европы и Северной Америки с оставляет 1 на 2000 — 2500 новорожденных. Так, например, в Ирландии частота муковисцидоза составляет 1: 1800 новорожденных, в Финляндии – 1: 26000. муковисцидоз крайне редок среди коренного населения Азии и Африки (менее 1 на 100 000 ) . По данным эпидемиологических исследований в России частота болезни в различных регионах колеблется от 1:8500 до 1:12900 новорождённых. Если оба родителя гетерозиготные (являются носителями мутировавшего гена), то риск рождения больного муковисцидозом ребёнка составляет 25 %. Носители только одного дефектного гена (аллели) не болеют муковисцидозом. По данным исследований частота гетерозиготного носительства патологического гена равна 2 — 5 %
Ежегодно в Москве рождается около 30 больных муковисцидозом , в России — 650, в США — 2000, во Франции, Англии, Германии — от 500 до 800, а в мире — более 45 000 больных детей. Это заболевание является важной медико-социальной проблемой, что связано, с одной стороны, с большими моральными, физическими и материальными затратами семьи, органов здравоохранения и общества в целом на диагностику, лечение, реабилитацию и социальную адаптацию больных, с другой стороны, с впечатляющими успехами в изучении этой проблемы, что дает толчок к развитию как фундаментальных, так и прикладных наук медицинского направления.
Микробиология и эпидемиология хронической респираторной инфекции при муковисцидозе
Спектр бактериальных патогенов при муковисцидозе довольно специфичен. В классическом варианте в раннем возрасте развивается инфекция, вызванная Staphylococcus aureus ( S . aureus ), затем с увеличением возраста присоединяется инфекция, обусловленная Haemophilus influenzae ( H . influenza е ) и Pseudomonas aeruginosa ( P . aeruginosa ). С конца 90 — х годов эпидемиология легочных инфекций у больных муковисцидозом стала значительно более сложной. Наряду с распространенными возбудителями, такими как S.aureus , H. influenza е и P.aeruginosa , в последние годы всё большее клиническое значение приобретают неферментирующие глюкозу грамотрицательные бактерии (НГОБ) Burkholderia cepacia complex ( B . cepacia complex ) , Stenotrophomonas maltophilia ( S . maltophilia ) , Achromobacter xylosoxidans ( A . xylosoxidans ), нетуберкулезные микобактерии (НТМБ). Помимо бактериальных агентов при исследовании респираторных биосубстратов нижних дыхательных путей больных МВ все чаще выделяют микромицеты .
 Частота выделения микромицетов из респираторных субстратов больных муковисцидозом варьирует от 6 до 57%. Средний возраст пациента на момент первого эпизода выделения микромицетов из респираторных субстратов составляет 12 лет, частота микотической колонизации увеличивается по мере взросления. Описано более 20 родов дрожжевых и мицелиальных микромицетов, полученных из мокроты и бронхо альвеолярного лаважа (БАЛ) больных муковисцидозом. Наиболее часто выделяют Aspergillus spp . -60% . В последнее десятилетие возросла частота выделения и других микромицетов, таких как Exophiala dermatitidis , Scedosporium spp , Rodotorula mucilaginosa , Fusarium spp . Rasamsonia argillacea , Penicillum emersonii и Acrophialophora fusispora были получены исключительно у больных муковисцидозом . Наибольшее клиническое значение имеет выявление в респираторных субстратах больных муковисцидозом грибов рода Aspergillu s . Выделение Candida spp . из мокроты и БАЛ свидетельствует о поверхностной колонизации дыхательных путей, не требующей медикаментозного лечения.
Частота выделения микромицетов из респираторных субстратов больных муковисцидозом варьирует от 6 до 57%. Средний возраст пациента на момент первого эпизода выделения микромицетов из респираторных субстратов составляет 12 лет, частота микотической колонизации увеличивается по мере взросления. Описано более 20 родов дрожжевых и мицелиальных микромицетов, полученных из мокроты и бронхо альвеолярного лаважа (БАЛ) больных муковисцидозом. Наиболее часто выделяют Aspergillus spp . -60% . В последнее десятилетие возросла частота выделения и других микромицетов, таких как Exophiala dermatitidis , Scedosporium spp , Rodotorula mucilaginosa , Fusarium spp . Rasamsonia argillacea , Penicillum emersonii и Acrophialophora fusispora были получены исключительно у больных муковисцидозом . Наибольшее клиническое значение имеет выявление в респираторных субстратах больных муковисцидозом грибов рода Aspergillu s . Выделение Candida spp . из мокроты и БАЛ свидетельствует о поверхностной колонизации дыхательных путей, не требующей медикаментозного лечения.
Роль других видов микромицетов в патологии легких у больных муковисцидозом изучена недостаточно. При несвоевременной диагностике поражения нижних дыхательных путей больных с муковисцидозом микромицетами и в отсутствие адекватного лечения в легких формируются проксимальные бронхоэктазы, отмечается быстрое прогрессирование бронхолегочного процесса , нарастание вентиляционных расстройств.
В настоящее время одной из главных причин ухудшения течения заболевания и летального исхода является инфекция, вызванная бактериями B. сepacia complex . Больные, инфицированные B. cepacia complex , являются источником инфекции и представляют опасность для других пациентов. В последние годы возросла клиническая значимость для жизни больных и других представителей грамотрицательных неферментирующих бактерий -Achromobacter spp . , S . maltophilia . Современная концепция поражения легких при муковисцидозе указывает, что определенную роль в повреждении легочной ткани играют иммунные процессы. Иммунологические нарушения значительно возрастают при длительной колонизации нижних дыхательных путей P. aeruginosa.
В процессе своего размножения микроколонии этого микроорганизма продуцируют вирулентные факторы, которые повреждают эпителий нижних дыхательных путей, стимулируют выработку медиаторов воспаления, повышают проницаемость капилляров, вызывают лейкоцитарную инфильтрацию. По данным Регистра 2015 г., в который включены данные 2 916 больных (2 877 живых и 39 умерших) , возраст больных колеблется от 0,1 до 6 6,0 лет. Средний возраст в 2015 году составил 12, 1 ± 9, 5 лет, медиана возраста – 9,7 (1 3 ,2) лет. Доля взрослых пациентов (≥ 18 лет) – 2 4,6 %.
Частота инфицирования дыхательных путей различной флорой представлена в порядке убывания: S. aureus – 5 6 , 0 %, P. aeruginosa (хроническое инфицирование) – 32,1 %, P.aeruginosa (интермиттирующее инфицирование) — 15,1%, B.cepacia complex – 6 , 6 %, метицилл ин — резистентный S.aureus ( MRSA ) — 6,4%, Achromobacter sp p . — 3, 9 %, S. maltophilia – 3,4 %, НТМБ — 0,9 %. При оценке микробиологического профиля респираторного тракта выявлено возрастание частоты высева грамотрицательной флоры с увеличением возраста больных. Наибольшая частота инфицирования S.aureus наблюдалась в возрастной группе 12 — 16 лет, где она составила 64,5%, P.aeruginosa в 24 — 28 лет с частотой 5 5 , 0 %, максимальная частота инфицирования В.сepacia со mplex в 2 4 — 2 8 лет – 2 2 , 6 %, S.maltophilia в 16 — 20 лет – 5 , 6 %, а частота обнаружения Achromobacter spp . достигала своего пика у пациентов старше 36 лет, где его частота составила 1 4 , 3 %. Данные о частоте инфицирования нижних дыхательных путей раз личной микрофлорой у пациентов с МВ в различных возрастных группах представлены на рис.1
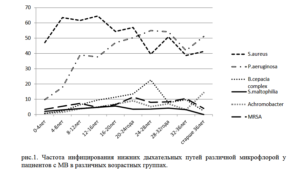
Данные о частоте выделения микромицетов из респираторного тракта больных муковисцидозом в национальном Регистре в настоящее время не отражены, тем не менее, результаты проведенного НИИ медицинской микологии им. П.Н. Кашкина в 2014 — 2016 гг. пилотного исследования свидетельствуют, что колонизация дыхательных путей Aspergillus spp . возникает у 22% больных муковисцидозом , а различные варианты аспергиллеза – у 9,2%. 010 20 30 40 50 60 70 S.aureus P.aeruginosa В. cepacia с omplex S.maltophilia Achromobacter MRSA 17 Микроорганизмы, инфицирующие нижние дыхательные пути больного муковисцидозом, определяют лечение, качество жизни, перспективы трансплантации и общую выживаемость. Точная и своевременная идентификация возбудителей инфекции дыхательных путей имеет значение для обеспечения своевременного начала адекватного лечения антибактериальными препаратами (АПБ), надлежащего микробиологического мониторинга с целью организации инфекционного контроля и профилактики распространения патогенных микроорганизмов среди больных муковисцидозом.
Микробиологическая диагностика
Задачами микробиологической диагностики хронической респираторной инфекции при муковисцидозе являются:
- Выделение и идентификация бактерий и грибов которые, колонизируя нижние дыхательные пути больных муковисцидозом, ведут к ухудшению дыхательной функции, могут быть источником инфицирования других пациентов с муковисцидозом и приводить к осложнениям после трансплантаций;
- Обеспечение раннего выявления первичной колонизации P.aerugino sa , B.cepacia соmplex и микромицетами [ 11 ];
- Предоставление рекомендаций для антимикробной терапии (профиль антибиотикочувствительности, выявление механизмов резистентности и проведение экспертной оценки результатов исследования).
- В таблице 1 представлены рекомендации по методам идентификации и определению чувствительности микроорганизмов, которые наиболее часто присутствуют в нижних дыхательных путях при хронических респираторных инфекциях больных с муковисцидозом.
Информацию по ДНК -диагностике можно посмотреть здесь
СКАЧАТЬ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО МУКОВИСЦИДОЗУ