 Резюме
Резюме
Цели и задачи. Изучить частоту случаев затруднения при обеспечении проходимости дыхательных путей и трудной интубации после появления и широкого распространения заместительной терапии у детей с мукополисахаридозом (МПС) в Австралии.
Краткая информация
За последние 20–25 лет достигнуты значительные успехи в лечении МПС — сейчас многим пациентам предлагают пересадку костного мозга или заместительную терапию ферментными препаратами (ЗТФП). Влияние этих методов лечения на частоту случаев затруднения при обеспечении проходимости дыхательных путей недостаточно изучено. Кроме этого, были разработаны методы анестезии и устройства для обеспечения проходимости дыхательных путей, которые, как считается, существенно повысили безопасность ведения этих пациентов во время анестезии, но систематического исследования их роли в лечении детей с МПС не проводилось.
Методы
Ретроспективный анализ амбулаторных карт и историй болезни 17 пациентов с МПС, которым проводили анестезию в Королевской детской больнице в период с января 1998 г. по январь 2011 г. Первичным критерием было число случаев трудной или неудавшейся интубации. Вторичным критерием была взаимосвязь между числом случаев трудной интубации и ЗТФП или трансплантацией костного мозга.
Результаты. Проанализирован 141 случай обеспечения анестезии при проведении 214 процедур у семнадцати пациентов. Трудная вентиляция через лицевую маску наблюдалась в 20 случаях (14,2%). Трудная интубация отмечена в 40 случаях (25%). В двух случаях провести интубацию не удалось (1,6%). Частота случаев трудной интубации составила 12% при МПС I типа, 35% при МПС II типа, 86,7% при МПС VI типа и 0% при МПС III и IV типов.
Заключение
Трансплантация кроветворных стволовых клеток в возрасте до 2 лет снижает число случаев трудной вентиляции через маску и трудной интубации у детей с МПС I типа. У пациентов с МПС II и VI типа ЗТФП была начата на более поздних стадиях заболевания. Проведенная терапия улучшила проходимость верхних дыхательных путей, но не уменьшила количество случаев затруднений при обеспечении проходимости дыхательных путей.
Введение
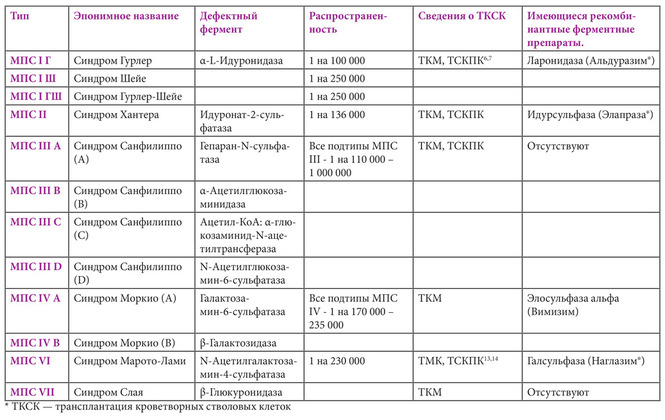
Мукополисахаридозами (МПС) называют группу из семи хронических прогрессирующих заболеваний с эпонимными названиями, вызываемых недостаточностью 11 различных лизосомальных ферментов, участвующих в катаболизме гликозаминогликанов (ГАГ) (табл. 1). Многие клинические проявления синдромов МПС могут стать причиной затруднений при проведении анестезии, в том числе серьезных проблем с проходимостью дыхательных путей (1–4). Уплотнение мягких тканей, увеличенный язык, короткая неподвижная шея, ограниченная подвижность шейного отдела позвоночника и височно-нижнечелюстных суставов затрудняют ларингоскопию и интубацию.
Табл. 1. Классификация и эпонимные названия мукополисахаридозов и показатели распространенности в Австралии. Мукополисахаридоз (МПС) V типа, ранее называвшийся синдромом Шейе, и МПС VIII типа в качестве названий заболеваний больше не используются. Исследования показали, что трансплантация кроветворных стволовых клеток (ТКСК) и костного мозга (ТКМ) или стволовых клеток пуповинной крови (ТСКПК) предотвращает развитие многих клинических проявлений тяжелых форм МПС I, VI и VII типов. Несмотря на предпринятые попытки, применение ТКСК не снижало степень неврологических и ортопедических нарушений при МПС II, III и IV типов, поэтому в настоящее время этот вид терапии не рекомендуется.
 Деформации позвоночника, гепатоспленомегалия, гранулематозное поражение тканей дыхательных путей и рецидивирующие легочные инфекции ухудшают респираторную функцию. При МПС I, IV и VI типов часто встречается дисплазия зубовидного отростка осевого позвонка и подвывих атлантоосевого сустава, обнаруживаемый при рентгенографии. Эти изменения могут приводить к смещению атланта кпереди и сдавливанию спинного мозга. Начало заместительной терапии рекомбинантными ферментными препаратами или трансплантация кроветворных стволовых клеток снижают накопление ГАГ в верхних дыхательных путях, однако сведения о влиянии этих видов терапии на частоту возникновения проблем с проходимостью дыхательных путей во время анестезии ограничены.
Деформации позвоночника, гепатоспленомегалия, гранулематозное поражение тканей дыхательных путей и рецидивирующие легочные инфекции ухудшают респираторную функцию. При МПС I, IV и VI типов часто встречается дисплазия зубовидного отростка осевого позвонка и подвывих атлантоосевого сустава, обнаруживаемый при рентгенографии. Эти изменения могут приводить к смещению атланта кпереди и сдавливанию спинного мозга. Начало заместительной терапии рекомбинантными ферментными препаратами или трансплантация кроветворных стволовых клеток снижают накопление ГАГ в верхних дыхательных путях, однако сведения о влиянии этих видов терапии на частоту возникновения проблем с проходимостью дыхательных путей во время анестезии ограничены.
Материалы и методы
Ретроспективное исследование было одобрено этическим комитетом Королевской детской больницы. Для исследования были выбраны дети с подтвержденным диагнозом мукополисахаридоза, поставленным на основании полного анамнеза, тщательного обследования, анализа на активность ферментов и молекулярно-генетического исследования. В группу исследования включали детей, чьи медицинские карты имелись в нашей больнице. Были изучены медицинские карты детей до 18 лет с МПС, которым выполняли анестезию для проведения терапевтических или диагностических процедур в период с января 1998 г. по январь 2011 г. В число собираемых демографических данных входили дата рождения, возраст, сведения о патологии, имевшейся на момент выполнения анестезии, нарушениях со стороны дыхательной системы, сердца и опорно-двигательного аппарата. Данные о метаболическом статусе содержали сведения о типе МПС, дате начала и виде лечения. Хирургический анамнез включал сведения о дате и типе процедуры, осложнениях в этот период и месте нахождения пациента после операции. В число регистрируемых анастезиологических параметров входили дооперационное обследование, оценка состояния дыхательных путей, применение особых устройств для обеспечения проходимости дыхательных путей при проведении анестезии, а также осложнения, связанные с попытками интубации, возникавшие во время операции и после нее.
«Трудные дыхательные пути» определялись как наличие проблем с вентиляцией через лицевую маску или обструкция верхних дыхательных путей во время анестезии. «Трудная интубация» определялась как клиническая ситуация, при которой опытный анестезиолог испытывает трудности с визуализацией структур гортани (третья или более высокая степень визуализации по шкале Кормака-Лехана), проводятся многократные попытки интубации (больше трех) или возникает необходимость в использовании дополнительного оборудования помимо ларингоскопа для прямой ларингоскопии. Неудавшейся интубацией считалась невозможность установить эндотрахеальную трубку в трахею.
Статистические данные
Исследование представляло собой описательный ретроспективный анализ, поэтому оценку объема выборки не проводили. Число участников исследования определялось количеством пациентов, получавших анестезию в указанный период, при условии, что в их истории болезни имелась анестезиологическая карта, которая была достаточно полной для получения необходимых данных.
Непрерывные переменные выражали как среднее ± стандартное отклонение или как медиану (межквартильный размах). Категориальные переменные выражали в виде частоты (%). Для сравнения относительных показателей применяли метод расчета критерия хи-квадрат. Непрерывные результаты с бинарными переменными сравнивали с помощью критерия Стьюдента в случае нормального распределения данных и критерия суммы рангов Уилкоксона в случае несимметричных данных.
Результат считали статистически значимым при значении P < 0,05. Затем значимые переменные подвергали множественному логистическому регрессионному анализу. Всю статистическую обработку проводили с использованием программного пакета STATA версии 10.0 (Stata Corp, College Station, Техас, США).
Результаты
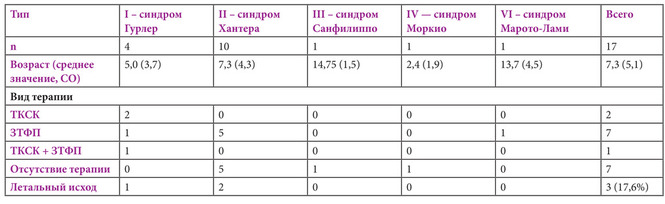
Проанализирован 141 случай обеспечения анестезии при проведении 214 процедур у семнадцати пациентов (табл. 2). Самому младшему пациенту было 2 месяца, а самому старшему — 18 лет. Пациентов распределили по группам в соответствии с видом лечения (отсутствие терапии, ЗТФП или ТКСК) и по типу МПС (I, II, III, IV и VI).
Нарушения со стороны сердца наблюдались у 16 пациентов (94%). Стеноз или утолщение створок митрального клапана наблюдались у 14 пациентов (82%), при этом у трех из них (18%) была умеренная или тяжелая митральная регургитация. Поражения аортального клапана наблюдались у 15 пациентов (88%), при этом у одного из них была среднетяжелая аортальная регургитация. У одного пациента до начала лечения имелась дилатационная кардиомиопатия. Состояние пациента сначала удалось стабилизировать с помощью ЗТФП и последующей трансплантации костного мозга, но после терапии антрациклином ситуация значительно ухудшилась. Поражения верхних дыхательных путей, сопровождающиеся апноэ во сне, имелись у шести пациентов (у четырех пациентов с МПС II типа, одного пациента с МПС I типа и одного с МПС III типа). У трех других пациентов отмечался громкий храп при нормальном сне. У шести пациентов были обнаружены отклонения от нормы в шейном отделе позвоночника по данным МРТ. Четырем пациентам МРТ исследование шейного отдела не проводилось, а у семи остальных отклонения на МРТ снимках не обнаружены. У трех пациентов имелось сдавление передних отделов спинного мозга мягкими тканями на уровне первого и второго шейных позвонков (два пациента с МПС I типа и один с МПС II типа), у двух пациентов наблюдалось значительное сдавливание спинного мозга в шейном отделе (один пациент с МПС II типа и один с МПС VI типа), а у одного пациента с МПС IV типа имелись гипоплазия зубовидного отростка, сдавливание продолговатого мозга и шейного отдела спинного мозга и стеноз позвоночного канала от первого до четвертого шейного позвонка.
Процедуры
Чаще всего (рис. 1) выполнялись процедуры, связанные с заболеваниями уха, горла и носа (ЛОР) (n = 44; 20,6%), пластические операции (n = 32; 15%), исследования методами лучевой диагностики (n = 36; 16,8%) и общие хирургические процедуры (n = 24; 11,2%). Средний возраст при первом проведении анестезии или хирургического вмешательства во всей популяции исследования составил 4,43 года (СО 3,58; диапазон 0,5–12 лет). Средний возраст пациентов, подвергавшихся ТКСК, на время первой процедуры составил 1,22 года (СО 0,69; диапазон 0,66–2 года), пациентов, получавших ЗТФП — 4,43 года (СО 3,5; диапазон 1–10 лет), а пациентов, не получавших лечения — 3,38 года (СО 4,26, диапазон 0,5–12 лет).
Анестезия
Из 141 случаев проведения анестезии, 108 процедур (76,6%) были проведены специалистами по детской анестезиологии, 11 процедур (7,8%) были проведены специалистами по анестезиологии не педиатрического профиля и 22 процедуры (15,6%) — анестезиологами-ординаторами. Индукция анестезии с помощью ингаляционных анестетиков выполнялась в 121 случаях (85,8%), в 112 (79,4%) из которых использовали севофлуран с кислородом и в 9 (6,4%) случаях — галотан с кислородом. Для внутривенной индукции анестезии в 17 случаях (12%) использовали пропофол, а в двух случаях (1,4%) — фентанил. Одному 6-недельному ребенку была проведена пластика двусторонней грыжи с применением спинальной анестезии при сохраненном сознании.
У девяти пациентов примерно в 20 случаях наблюдалась либо трудная вентиляция дыхательным мешком через маску, либо обструкция дыхательных путей во время индукции анестезии. Во всех случаях трудности удалось преодолеть за счет использования ларингеальной маски, носового или ротового воздуховода. Трудная вентиляция через маску имела место у 4,2% пациентов после трансплантации костного мозга, у 12,5% пациентов, получающих ЗТФП, и у 26,7% пациентов, не получавших никакого лечения.
Табл. 2. Демографические данные детей с мукополисахаридозом, подвергавшихся анестезии. Возраст пациентов, которым проводились хирургические вмешательства, представлен в виде среднего значения со стандартным отклонением (СО). Вариантами терапии были трансплантация кроветворных стволовых клеток (ТКСК), заместительная терапия рекомбинантными ферментными препаратами (ЗТФП) и только поддерживающее лечение (отсутствие терапии). Один пациент получал ЗТФП до и после ТКСК. Три пациента умерли во время периода исследования от осложнений, не связанных ни с анестезией, ни с хирургической процедурой.
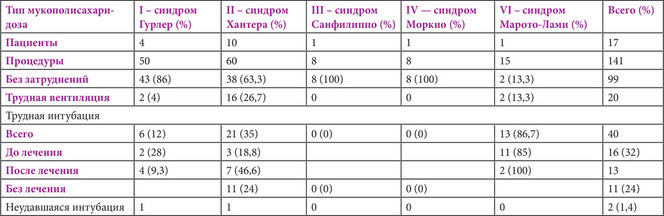
 У пациентов с МПС II типа трудная вентиляция через маску наблюдалась в 26,7% случаев, а у пациентов с МПС I типа — в 4% случаев. Основными средствами обеспечения проходимости дыхательных путей, применявшимися в ходе 141 процедуры, были: лицевая анестезиологическая маска в 14 случаях (9,9%), ларингеальная маска в 60 случаях (42,6%), эндотрахеальная трубка в 51 случае (36,2%) и существующая трахеостома у 15 пациентов (10,6%). Из 59 попыток интубации трахеи 51 оказалась успешной. У шести пациентов после неудачи с визуализацией голосовой щели была использована ларингеальная маска, при этом в двух случаях выполнить интубацию не удалось. Во время шести процедур анестезии интубацию трахеи проводили с помощью оптоволоконного бронхоскопа (в 4 случаях по выбору анестезиолога и в 2 случаях из-за возникновения трудностей с обеспечением проходимости дыхательных путей). Ларингеальную маску использовали в качестве проводника для бронхоскопа во время пяти процедур анестезии, а во время одной процедуры использовали фибробронхоскоп, который вводили через нос.
У пациентов с МПС II типа трудная вентиляция через маску наблюдалась в 26,7% случаев, а у пациентов с МПС I типа — в 4% случаев. Основными средствами обеспечения проходимости дыхательных путей, применявшимися в ходе 141 процедуры, были: лицевая анестезиологическая маска в 14 случаях (9,9%), ларингеальная маска в 60 случаях (42,6%), эндотрахеальная трубка в 51 случае (36,2%) и существующая трахеостома у 15 пациентов (10,6%). Из 59 попыток интубации трахеи 51 оказалась успешной. У шести пациентов после неудачи с визуализацией голосовой щели была использована ларингеальная маска, при этом в двух случаях выполнить интубацию не удалось. Во время шести процедур анестезии интубацию трахеи проводили с помощью оптоволоконного бронхоскопа (в 4 случаях по выбору анестезиолога и в 2 случаях из-за возникновения трудностей с обеспечением проходимости дыхательных путей). Ларингеальную маску использовали в качестве проводника для бронхоскопа во время пяти процедур анестезии, а во время одной процедуры использовали фибробронхоскоп, который вводили через нос.
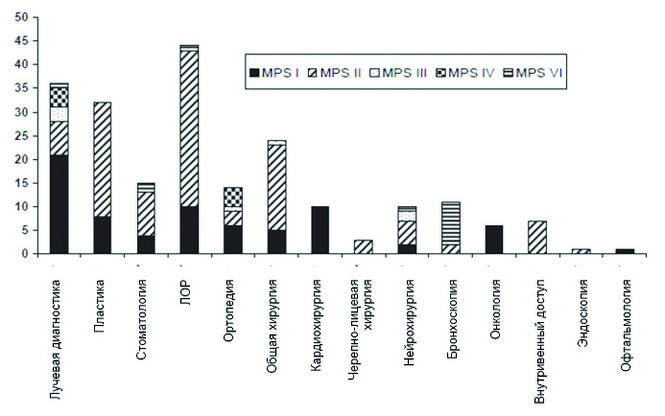 Рис. 1. Сведения о хирургических вмешательствах по каждому типу мукополисахаридоза
Рис. 1. Сведения о хирургических вмешательствах по каждому типу мукополисахаридоза
Количество случаев трудной интубации сопоставляли с типом МПС, видом терапии и возрастом пациента (табл. 3). У 12 пациентов были зарегистрированы 40 случаев значительных проблем с поддержанием проходимости дыхательных путей. Общая частота случаев трудной интубации составила 39 из 141 процедур анестезии (27,6%), при этом в 2 случаях из этих 141 процедур интубация не удалась (1,4%). Наибольшее число случаев трудной интубации было зарегистрировано у пациентов с МПС II типа (35%). Одному пациенту с МПС VI типа, которому на тот момент было 7 лет, из-за неудавшейся экстубации после операции потребовалось провести трахеостомию. Чтобы оценить накопление ГАГ в трахее ребенка, пришлось несколько раз прибегнуть к бронхоскопии жестким бронхоскопом, причем при всех последующих процедурах у этого пациента была затруднена визуализация гортани.
В двух случаях проведения анестезии неудавшаяся интубация стала причиной отмены процедуры.
Табл. 3. Обеспечение проходимости дыхательных путей и возникшие осложнения «Трудная вентиляция через маску» определялась как наличие проблем с вентиляцией через лицевую маску, в том числе потребовавших применения воздуховода Гведела, назофарингеального воздуховода или ларингеальной маски для преодоления обструкции верхних дыхательных путей во время индукции анестезии. «Трудная интубация» определялась как наличие трудностей с визуализацией структур гортани (третьей или более высокой степени по шкале Кормака-Лехана), многократные попытки интубации или необходимость в применении дополнительного оборудования помимо прямого ларингоскопа.
 В одном из этих случаев анестезию 6-недельному ребенку с МПС I типа проводил анестезиолог без специализации по педиатрии. Маловероятно, что трудности с интубацией у этого пациента были вызваны накоплением ГАГ в верхних дыхательных путях. Во втором случае ребенку с МПС II типа предстояло установить устройство для центрального сосудистого доступа. Несмотря на многократные попытки с применением обычного ларингоскопа и ларингоскопа МакКоя, была обеспечена лишь IV степень визуализации гортани. Визуализация была достигнута с помощью ларингеальной маски, но ввести эндотрахеальную трубку в трахею не удалось.
В одном из этих случаев анестезию 6-недельному ребенку с МПС I типа проводил анестезиолог без специализации по педиатрии. Маловероятно, что трудности с интубацией у этого пациента были вызваны накоплением ГАГ в верхних дыхательных путях. Во втором случае ребенку с МПС II типа предстояло установить устройство для центрального сосудистого доступа. Несмотря на многократные попытки с применением обычного ларингоскопа и ларингоскопа МакКоя, была обеспечена лишь IV степень визуализации гортани. Визуализация была достигнута с помощью ларингеальной маски, но ввести эндотрахеальную трубку в трахею не удалось.
Влияние разных видов лечения на частоту затруднений с обеспечением проходимости дыхательных путей оценивали с помощью регрессионного анализа. Пациенты с МПС II типа начинали получать ЗТФП в среднем в возрасте 9,4 года (диапазон 8–13 лет). Вероятность трудной интубации для пациентов, получающих ЗТФП, оказалась в 3,09 раза выше, чем для пациентов, не получавших никакого лечения (95% ДИ: 0,78–12,28; P = 0,109). Вероятность трудной интубации для пациентов, перенесших ТКСК, составила 0,36 от таковой для пациентов, не получавших никакого лечения (95% ДИ: 0,08–1,54; P = 0,17).
Для оценки влияния фенотипа МПС на частоту проблем с обеспечением ПДП также применяли регрессионный анализ. Вероятность трудной интубации для пациентов с МПС II типа оказалась выше, чем для пациентов с МПС I типа (P = 0,02). Найденное отношение шансов составило 3,95 (95% ДИ: 1,27–12,29), однако доверительный интервал оказался очень широким. Провести сравнение с другими типами МПС не удалось из-за недостаточного количества пациентов в этих группах.
Частота случаев трудной интубации увеличивается с возрастом, но влияние этого фактора невелико. Расчет методом логистической регрессии с поправкой на повторные процедуры анестезии показал, что в среднем вероятность трудной интубации увеличивается на 19% с каждым последующим годом жизни (95% ДИ: 2–40%, P = 0,026). В группах, получавших лечение (ЗТФП и ТКСК), расчетное изменение вероятности трудной интубации сократилось до 15% с каждым последующим годом жизни (95% ДИ: от –1% до 33%, P = 0,06).
Осложнения в периоперативном периоде
Зарегистрированы три события, связанные с проходимостью дыхательных путей, имевшие место во время операции (два эпизода гипоксемии и один эпизод смещения ларингеальной маски). Все три эпизода имели место у детей с МПС II типа. Проблемы с обеспечением ПДП в периоперативном периоде отмечены в 17 из 141 случая проведения анестезии (12,1%). У пяти пациентов (3,5%) во время пребывания в палате посленаркозного наблюдения развилась обструкция дыхательных путей, но ни в одном из случаев повторной интубации не потребовалось. Во время нахождения в операционной после завершения анестезии, у семи пациентов (5%) возникла десатурация (у двух пациентов до SpO2 < 90%), у четырех пациентов (2,8%) наблюдался стридор после экстубации, а у одного (0,9%) была длительная гиповентиляция.
 У одного пациента (0,9%) без очевидных причин развилась наджелудочковая тахикардия, но состояние нормализовалось без лечебных мероприятий. Шестьдесят одна процедура анестезии (43,3%) проводилась в условиях дневного стационара, в 71 случаях (50,4%) пациенты после вмешательства поступали в общую палату хирургического отделения, а девять пациентов (6,4%) были переведены из операционной в детское отделение интенсивной терапии (ДОИТ). Четыре пациента поступали в ДОИТ в общей сложности в девяти случаях. Один пациент с МПС VI типа был переведен в ДОИТ, так как анестезиолог считал, что его дыхательные пути сильно пострадали после многократных попыток обеспечить эндотрахеальную интубацию, поэтому экстубацию следовало отложить. Второй пациент с МПС II типа, у которого наблюдалась обструкция верхних дыхательных путей, был переведен в ДОИТ после операции по уменьшению языка, так как ему требовалось проведение искусственной вентиляции легких до отложенной экстубации. Обоим пациентам впоследствии не удалось провести экстубацию и в обоих случаях пришлось прибегнуть к трахеостомии. Один пациент с МПС I типа и дилатационной кардиомиопатией вследствие приема антрациклина, был переведен из общей палаты в ДОИТ, после того как у него развилась тяжелая сердечная недостаточность. В качестве метода вспомогательного кровообращения пациенту проводилась экстракорпоральная мембранная оксигенация (ЭКМО). Один пациент с МПС II типа и хронической болезнью легких был помещен в отделение для наблюдения. За период, охватываемый исследованием, три ребенка умерли. Один 2-летний ребенок с МПС I типа умер, несмотря на проведение ЭКМО, от осложнений, связанных с кардиомиопатией, а два ребенка с МПС II типа умерли от тяжелой дыхательной недостаточности (один в возрасте 18, а второй в возрасте 15 лет).
У одного пациента (0,9%) без очевидных причин развилась наджелудочковая тахикардия, но состояние нормализовалось без лечебных мероприятий. Шестьдесят одна процедура анестезии (43,3%) проводилась в условиях дневного стационара, в 71 случаях (50,4%) пациенты после вмешательства поступали в общую палату хирургического отделения, а девять пациентов (6,4%) были переведены из операционной в детское отделение интенсивной терапии (ДОИТ). Четыре пациента поступали в ДОИТ в общей сложности в девяти случаях. Один пациент с МПС VI типа был переведен в ДОИТ, так как анестезиолог считал, что его дыхательные пути сильно пострадали после многократных попыток обеспечить эндотрахеальную интубацию, поэтому экстубацию следовало отложить. Второй пациент с МПС II типа, у которого наблюдалась обструкция верхних дыхательных путей, был переведен в ДОИТ после операции по уменьшению языка, так как ему требовалось проведение искусственной вентиляции легких до отложенной экстубации. Обоим пациентам впоследствии не удалось провести экстубацию и в обоих случаях пришлось прибегнуть к трахеостомии. Один пациент с МПС I типа и дилатационной кардиомиопатией вследствие приема антрациклина, был переведен из общей палаты в ДОИТ, после того как у него развилась тяжелая сердечная недостаточность. В качестве метода вспомогательного кровообращения пациенту проводилась экстракорпоральная мембранная оксигенация (ЭКМО). Один пациент с МПС II типа и хронической болезнью легких был помещен в отделение для наблюдения. За период, охватываемый исследованием, три ребенка умерли. Один 2-летний ребенок с МПС I типа умер, несмотря на проведение ЭКМО, от осложнений, связанных с кардиомиопатией, а два ребенка с МПС II типа умерли от тяжелой дыхательной недостаточности (один в возрасте 18, а второй в возрасте 15 лет).
Обсуждение результатов
Проведенное исследование показало, что частота проблем с обеспечением ПДП до сих пор довольно высока, несмотря на появление таких методов лечения, как трансплантация костного мозга и заместительная терапия рекомбинантными ферментными препаратами. К числу факторов, связанных с повышенным риском проблем с обеспечением ПДП у детей, относится наличие МПС II и IV типа, начало ЗТФП на более поздних стадиях заболевания, а также более старший возраст. Частота случаев трудной интубации у детей с МПС I типа, которым трансплантация костного мозга была проведена на ранних стадиях заболевания, была значительно ниже по сравнению с ранее сообщенными данными. Результаты исследования согласуются с ранее полученными данными, которые указывают на то, что дети с МПС I, II или VI типа были особенно подвержены риску возникновения проблем с обеспечением ПДП во время анестезии. В обзоре, посвященном проведению анестезии у детей с 1983 по 1993 гг. в Мельбурне, описаны 28 пациентов, которым потребовалась анестезия в 99 случаях для выполнения 115 процедур (3). Трудная интубация отмечена у 72% пациентов с МПС II типа, у 40% пациентов с МПС I типа и у 56% пациентов с МПС VI типа. Частота случаев неудавшейся интубации у пациентов с МПС I типа составила 29% (у двух из семи пациентов). В обзоре сообщалось также, что проблемы с обеспечением ПДП усугублялись с возрастом пациентов. Walker (5) в своей работе о группе пациентов из Манчестера привел данные о проблемах с проходимостью дыхательных путей у детей с МПС, которым проводились хирургические вмешательства в период с 1988 по 1991 гг.
Проанализировано 89 случаев обеспечения анестезии при проведении 110 процедур у тридцати четырех пациентов. Общая частота случаев трудной интубации у детей с мукополисахаридозами составила 25%. При этом, однако, у детей с МПС I типа трудная интубация наблюдалась в 54% случаев, а в 23% случаев интубация не удалась.
Меньшая частота проблем с проходимостью дыхательных путей при проведении анестезии, наблюдавшаяся в данном исследовании, скорее всего, объясняется влиянием заместительной терапии ферментными препаратами или аллогенной трансплантации костного мозга (6-9) на прогрессирование заболевания у детей с МПС. Трансплантация кроветворных стволовых клеток из пуповинной крови или костного мозга применяется в лечебных целях с 1980 г. (10). У пациентов с МПС I типа ТКСК изменяет характер течения заболевания — позволяет устранить гепатоспленомегалию, стабилизировать сердечные заболевания и снизить степень обструкции дыхательных путей (11). Считается, что положительный эффект ТКСК объясняется замещением дефектных макрофагов донорскими макрофагами из костного мозга, которые становятся постоянным источником нормальных ферментов, способных поступать к различным участкам накопления ГАГ. На сегодняшний день в Австралии пациентам с МПС проведено 18 трансплантаций кроветворных стволовых клеток (6). В Австралии ТКСК преимущественно предлагается детям до 2 лет с тяжелой неврологической формой МПС I типа, так как этот вид терапии замедляет свойственный этой форме нейродегенеративный процесс. В последнее время ТКСК применяют в сочетании с ЗТФП, назначаемой в периоперативном периоде, поскольку такой режим лечения может быть более эффективным с точки зрения восполнения дефицита ферментов до тех пор, пока не наладится их эндогенная выработка. В отличие от МПС I типа, ТКСК не предотвращает нейродегенерацию у детей с другими типами МПС (II или III), поэтому в этих случаях не рекомендуется. В работе Turbeville (12) сообщается о системном клиническом улучшении у 45 пациентов с МПС VI типа, которым была проведена аллогенная ТКСК в период с 1982 по 2007 гг.
Трансплантация кроветворных стволовых клеток
Сведения о влиянии данного вида терапии на развитие осложнений при проведении анестезии ограничены. В работе King (13) описаны случаи трудной ларингоскопии и затруднения при обеспечении проходимости дыхательных путей у семи из восьми пациентов (два с МПС I и шесть с МПС II типа), которым проводилась трансплантация амниона. Предполагалось, что подкожная имплантация амниотической мембраны может компенсировать недостаток ферментов у пациентов с МПС. К сожалению, имплантация амниона не обеспечивает долговременной коррекции недостаточности лизосомальных ферментов и не приводит к положительным изменениям в функции внутренних органов. Mahoney (10) и Walker (15) высказали мнение, что регрессия накоплений ГАГ в мягких тканях после ТКСК не сопровождается сокращением числа случаев трудной интубации. Mahoney и Soni (10) описали 35 пациентов (63% с МПС I типа и 20% с МПС II типа), которым были проведены 150 процедур анестезии после ТКСК. Из текста неясно, когда проводилась анестезия по отношению ко времени ТКСК, однако то, что в 43% случаев потребовалось применение катетера Хикмана для обеспечения центрального венозного доступа, позволяет предположить, что анестезия предшествовала ТКМ.
У пациентов с МПС I типа трудная интубация наблюдалась в 41% случаев, а у пациентов с МПС II типа — в 71% случаев. В работе Belani et al описаны 30 детей с МПС (21 с МПС I типа и пять с МПС III типа), 28 из которых была проведена ТКМ. У 15 из этих 30 пациентов имелась обструкция верхних дыхательных путей, у 35% наблюдалась трахеомаляция или сужение трахеи. Вскоре после ТКМ у всех детей, в анамнезе которых имелись сведения о наблюдавшихся до ТКМ обструктивном апноэ или десатурации, было отмечено заметное ослабление симптомов заболевания, кроме того автор отметил у них значительное улучшение визуализации гортани.
В работе Yeung описана группа из 27 пациентов, которым была выполнена трансплантация костного мозга (восемь с МПС I, три с МПС I Ш, пять с МПС II типа, один с болезнью I-клеток (муколипидоз II типа), один с МПС III и один с МПС VI типа). До ТКМ у 19 из 27 пациентов (70%) наблюдалась клинически значимая обструкция верхних дыхательных путей, установленная по результатам полисонмографии или по наличию эпизодов десатурации. Успешное приживление трансплантата привело к существенному ослаблению симптомов обструкции у 13 из 14 пациентов (16).
Заместительная терапия ферментными препаратами
В исследуемой группе ЗТФП не снижала частоту затруднений с обеспечением проходимости дыхательных путей. По нашим данным, частота случаев трудной интубации у детей, получающих ЗТФП, была в три раза выше, причем эта зависимость была особенно заметна у более старших детей с МПС II типа. Известная связь между трудной интубацией и МПС II типа была подтверждена четырехкратным увеличением вероятности этого осложнения у детей с МПС II типа в сравнении с МПС I типа. Повышенная частота проблем с обеспечением ПДП у детей, получающих ЗТФП, может объясняться тем, что заместительную терапию применяли на поздних стадиях заболевания, когда уже имелись значительные накопления ГАГ. Пациенты исследуемой группы начинали получать ЗТФП в среднем в возрасте 11,1 года, в то время как ТКМ выполняли в среднем в возрасте 1,65 года. В Австралии пациенты с МПС I, II и VI типа получают заместительную терапию рекомбинантными ферментными препаратами в рамках Программы обеспечения жизненно необходимыми препаратами. Ларонидаза (Альдуразим®), препарат, предназначенный для лечения МПС I типа, был разрешен к применению в 2007 г., идурсульфаза (Элапраза®), препарат для лечения МПС II типа, и галсульфаза (Наглазим®) для лечения МПС VI типа разрешены к применению в 2008 г. Недостаточная обеспеченность ферментными препаратами в Австралии в период исследования привела к тому, что 34 процедуры (35%) были выполнены до начала эффективного лечения у тех пациентов, которые впоследствии начали получать ЗТФП.
Результаты четырех исследований (11,17–19) показывают, что начало ЗТФП с 3-месячного возраста позволяет существенно снизить скорость накопления субстрата и прогрессирования нарушений функций органов у детей с МПС II типа. Mendelsohn (20) описал 527 пациентов с МПС II типа, получавших идурсульфазу (Элапраза®), по данным реестра больных с синдромом Хантера (Hunter Outcome Survey).
Проблемы с интубацией были зарегистрированы у 74 из 428 пациентов (22%), а 14 пациентам не удалось провести экстубацию (3,7%). До постановки диагноза трудная интубация была отмечена у 70 пациентов (18,6%), а проблемы с экстубацией возникли у 13 пациентов (7,7%).
Возраст
В исследуемой группе наблюдалась значительная корреляция между частотой случаев трудной интубации и увеличением возраста пациентов. Такая зависимость согласуется с некоторыми предыдущими сообщениями (3, 13, 21), но противоречит данным, представленным в других работах (2, 10). В работе Belani (21) приведены данные о повышении частоты трудной интубации у детей старше 23 месяцев и с массой тела более 12 кг. Напротив, Mahoney (10) в своей работе сообщил об отсутствии изменений в частоте случаев трудной интубации с увеличением возраста у 82% пациентов. У трех детей с МПС I типа проблемы с интубацией уменьшились, а у 2 детей ситуация ухудшилась. В группе пациентов, исследованной Baines (2), проблемы с обеспечением ПДП наблюдались в 33% случаев у детей младше года и в 42% случаев у детей старше 4 лет. Никто из детей в этой группе не получал ни ЗТФП, ни ТКСК.
Устройства для обеспечения проходимости дыхательных путей
В ранее описанных группах пациентов (2–4, 10) для обеспечения проходимости дыхательных путей преимущественно использовали эндотрахеальную трубку, при этом доля успешных интубаций составляла от 38 до 77%. В данной группе пациентов анестезиологи использовали обычный ларингоскоп, так как видеоларингоскопы для прямой ларингоскопии начали применяться в нашем отделении лишь недавно. Стандартная ларингеальная маска была единственным надгортанным устройством, которое применялось у этой группы пациентов. Данные Walker (22) свидетельствуют о целесообразности использования этого воздуховода как в качестве основного средства обеспечения проходимости дыхательных путей, так и в качестве проводника для оптоволоконной интубации у детей с МПС.
Хирургические вмешательства
Пациенты из исследованной нами группы поступали в больницу для проведения различных процедур, необходимых для мониторинга прогрессирования заболевания, а также для лечения с осложнениями МПС. Распределение по типам хирургических процедур было таким же, как в как базе данных реестра больных с синдромом Хантера (Hunter Outcome Survey) (20). В данной группе 487 пациентам, получавшим идурсульфазу (Элапразу®) в качестве терапии МПС II типа, были проведены 2067 хирургических вмешательств. Наиболее частой процедурой была миринготомия с введением дренажной трубки (51,7%), следующими по распространенности были пластика грыжи (50,3%), удаление аденоидов (50,1%), удаление миндалин (35,1%) и декомпрессия нерва в запястном канале (18,5%). Сходные данные приведены в работе Moores, где отмечено, что наиболее частыми хирургическими вмешательствами были операции на ЛОР-органах (37%), радиохирургические операции (19%) и ортопедические операции (11%).
Осложнения
В отличие от ряда других изученных групп пациентов, в исследуемой группе не наблюдалось значительных проблем с проходимостью дыхательных путей. Имеются сообщения о следующих осложнениях, связанных с проведением анестезии у пациентов с МПС: неудавшиеся попытки обеспечить проходимость дыхательных путей (23), смерть из-за отсутствия возможности интубации, ситуация, в которой не удалось провести вентиляцию (24), постобструктивный отек легких (25, 26), аритмия (27) и остановка сердца во время операции (28).
Ограничения
Выводы по результатам настоящего исследования имеют ряд ограничений. Дизайн исследования был основан на точности записей в анестезиологической карте. Поскольку сведения о том, легкой или трудной была интубация, брали из анестезиологических карт, эти данные были субъективным и менялись в зависимости от опытности выполнявшего манипуляцию анестезиолога. Во многих случаях анестезия требовалась для небольших и неинвазивных процедур и часто проводилась с использованием надгортанных воздуховодов, при этом попытки интубации трахеи не предпринимались. В результате у этой когорты пациентов частота проблем с обеспечением ПДП и других осложнений может быть занижена. Кроме того, данная когорта представляла собой особую группу пациентов, направленных в специализированный центр. Данную выборку нельзя считать репрезентативной в отношении всех детей с МПС, которым проводилась анестезия.
Выводы
Частота трудной интубации у детей с МПС II типа по-прежнему в двадцать раз выше, чем у других детей такого же возраста и с такой же массой тела. Проведение ТКСК у детей с МПС I типа до того, как им исполнится 2 года, не только замедляет прогрессирование заболевания, но и снижает частоту проблем с обеспечением ПДП. Влияние ЗТФП на обеспечение проходимости дыхательных путей нельзя адекватно оценить, так как пациенты из исследуемой группы начали получать препараты в том возрасте, когда из-за накопления ГАГ уже развились серьезные нарушения функций органов. Если бы терапия рекомбинантными ферментами была начата намного раньше, возможно, ее влияние было бы более заметным, чем было показано в этом исследовании.
Благодарности: 1.) Настоящее исследование проводилось при поддержке Программы правительства штата Виктория по поддержке деятельности инфраструктуры (OIS — Operational Infrastructure Support); 2.) Перевод данной статьи — Татьяна Щербаченко (Благотворительное сообщество переводчиков «Настоящее будущее»).
Конфликт интересов: Заявлено об отсутствии каких-либо конфликтов интересов.
Список литературы
- Kempthorne PM, Brown TC. Anaesthesia and the mucopolysaccharidoses: a survey of techniques and problems. Anaesth Intensive Care 1983; 11: 203-207.
- Baines D, Keneally J. Anaesthetic implications of the mucopolysaccharidoses: a fifteen-year experience in a children’s hospital. Anaesth Intensive Care 1983; 11: 198-202.
- Moores C, Rogers JG, McKenzie IM et al. Anaesthesia for children with mucopolysac- Anaesth Intensive Care 1996; 24: 459-463.
- Herrick IA, Rhine EJ. The mucopolysac-charidoses and anaesthesia: a report of clinical experience. Can J Anaesth 1988; 35: 67– 73.
- Walker RW, Darowski M, Morris P et al. Anaesthesia and mucopolysaccharidoses. A review of airway problems in children. Anaesthesia 1994; 49: 1078-1084.
- Moore AS, Shaw PJ, Hallahan AR et al. Haemopoietic stem cell transplantation for children in Australia and New Zealand, 1998–2006: a report on behalf of the Australasian Bone Marrow Transplant Recipient Registry and the Australian and New Zealand Children’s Haematology Oncology Group. Med J Aust 2009; 190: 121-125.
- Muenzer J, Fisher A. Advances in the treatment of mucopolysaccharidosis type I. N Engl J Med 2004; 350: 1932-1934.
- Muenzer J, Wraith JE, Clarke LA. Muco-polysaccharidosis I: management and treatment guidelines. Pediatrics 2009; 123: 19-29.
- Muenzer J, Gucsavas-Calikoglu M, McCandless SE et al. A phase I/II clinical trial of enzyme replacement therapy in mu-copolysaccharidosis II (Hunter syndrome). Mol Cancer Ther 2007; 90: 329-337.10 Mahoney A, Soni N, Vellodi A. Anaesthesia and the mucopolysaccharidoses: a review of patients treated by bone marrow transplantation. Paediatr Anaesth 1992; 2: 317-324.
- Muenzer J, Beck M, Giugliani R et al. Idur-sulfase treatment of Hunter syndrome in children younger than 6 years: results from the Hunter Outcome Survey. Genet Med 2011; 13: 102-109.
- Turbeville S, Nicely H, Rizzo JD et al. Clinical outcomes following hematopoietic stem cell transplantation for the treatment of mucopolysaccharidosis VI. Mol Genet Metab 2011; 102: 111-115.King DH, Jones RM, Barnett MB. Anaesthetic considerations in the mucopolysac- Anaesthesia 1984; 39: 126-131.
- Muenzer J, Neufeld EF, Constantopoulos G et al. Attempted enzyme replacement using human amnion membrane implantations in mucopolysaccharidoses. J Inherit Metab Dis 1992; 15: 25-37.
- Walker RW, Dearlove OR. Anaesthesia for children with mucopolysaccharidoses. Anaesth Intensive Care 1997; 25: 197-198.
- Yeung AH, Cowan MJ, Horn B et al. Airway management in children with muco-polysaccharidoses. Arch Otolaryngol Head Neck Surg 2009; 135: 73-79.
- Tylki-Szymanska A, Jurecka A, Zuber Z et al. Enzyme replacement therapy for mu-copolysaccharidosis II from 3 months of age: a 3-year follow-up. Acta Paediatr 2012; 101: e42–47.
- McGill JJ, Inwood AC, Coman DJ et al. Enzyme replacement therapy for mucopoly-saccharidosis VI from 8 weeks of age – a sibling control study. Clin Genet 2010; 77: 492-498.
- Furujo M, Kubo T, Kosuga M et al. Enzyme replacement therapy attenuates disease progression in two Japanese siblings with mucopolysaccharidosis type VI. Mol Genet Metab 2011; 104: 597-602.
- Mendelsohn NJ, Harmatz P, Bodamer O et al. Importance of surgical history in diagnosing mucopolysaccharidosis type II (Hunter syndrome): data from the Hunter Outcome Survey. Genet Med 2010; 12: 816–
- Belani KG, Krivit W, Carpenter BL et al. Children with mucopolysaccharidosis: peri-operative care, morbidity, mortality, and new findings. J Pediatr Surg 1993; 28: 403– 408; discussion 08-10.
- Walker RW, Allen DL, Rothera MR. A fibreoptic intubation technique for children with mucopolysaccharidoses using the laryn-geal mask airway. Paediatr Anaesth 1997; 7: 421-426.
- Gaitini L, Fradis M, Vaida S et al. Failure to control the airway in a patient with Hunter’s syndrome. J Laryngol Otol 1998; 112: 380-382.
- Chen YL, Wu KH. Airway management of patients with craniofacial abnormalities: 10-year experience at a teaching hospital in Tai J Chin Med Assoc 2009; 72: 468-470.
- Walker RW, Colovic V, Robinson DN et al. Postobstructive pulmonary oedema during anaesthesia in children with mucopolysac-charidoses. Paediatr Anaesth 2003; 13: 441– 447.
- Wilder RT, Belani KG. Fiberoptic intubation complicated by pulmonary edema in a 12-year-old child with Hurler syndrome. Anesthesiology 1990; 72: 205-207.
- Toda Y, Takeuchi M, Morita K et al. Complete heart block during anesthetic management in a patient with mucopolysac-charidosis type VII. Anesthesiology 2001; 95: 1035-1037.
- Seyedhejazi M, Sheikzadeh D, Sharabiani B. Cardiac arrest in a case of mucopolysac-charidosis after tracheostomy. J Cardiovasc Thorac Res 2010; 2: 51-53.






